ADA 2026 §2|糖尿病的診斷與分類
KEY TAKEAWAYS
- 糖尿病診斷四選一:A1C ≥ 6.5%、FPG ≥ 126 mg/dL(≥ 7.0 mmol/L,禁食 ≥ 8 h)、75-g OGTT 2-h PG ≥ 200 mg/dL(≥ 11.1 mmol/L),或具有典型高血糖症狀/高血糖危症時 random PG ≥ 200 mg/dL。三項實驗室標準在無不模糊高血糖時須兩次異常結果(同次抽血兩項不同檢查、或同檢查兩個時間點)才能確診。
- 糖尿病前期:A1C 5.7–6.4%(39–47 mmol/mol)、IFG(FPG 100–125 mg/dL)、IGT(75-g OGTT 2-h PG 140–199 mg/dL)。三項定義不全等價:T2D 一級預防介入(lifestyle、metformin)的證據主要來自 IGT ± IFG 族群,對單獨 IFG 或 A1C 定義之糖尿病前期效益較不確定。
- 三檢查異質性:FPG 與 A1C 易行、低變異;2-h PG 敏感度最高但作業繁瑣,是 cystic fibrosis–related diabetes(CFRD)與 posttransplantation diabetes mellitus(PTDM)的首選篩檢。OGTT 前 3 日須維持每日碳水 ≥ 150 g,否則可能偽陽。
- A1C 須採 NGSP 認證、追溯至 DCCT;POC 機型限於 CLIA 中等以上認證實驗室且 FDA 核准診斷用途。當 hemoglobin variants(如 sickle cell trait)、G6PD 缺乏(非裔男性 G202A 同合子可降 A1C 約 0.8%)、貧血、慢性腎臟病/透析、HIV、erythropoietin 使用、妊娠等改變紅血球生命週期時,須改用血糖標準。
- 診斷分類:T1D(自體免疫 β 細胞破壞 → 絕對胰島素缺乏,含 LADA)、T2D(β 細胞胰島素分泌進行性下降,常合併胰島素阻抗)、其他特異型(單基因型、外分泌胰臟疾病、藥物/化學物誘發)、GDM(妊娠中後期新發、孕前未明顯糖尿病者)。臨床上 T1D 與 T2D 不再以年齡作硬性界限。
- T1D 三階段:Stage 1 = 兩個以上 islet 自體抗體+正常血糖;Stage 2 = 多抗體+dysglycemia 但未達糖尿病;Stage 3 = 顯性高血糖。Stage 1 的 5 年發病率約 44%,Stage 2 進展至 Stage 3 的 2 年風險約 60%、5 年風險約 75%。
- T1D 自體抗體篩檢:GAD(首選)、IA-2、ZnT8、IAA。家族史或高遺傳風險者建議篩檢;單一 IA-2 抗體陽性者風險與多抗體陽性者相當,須等同密切追蹤。確診多抗體者可考慮 teplizumab(FDA 核可延緩 Stage 3)或轉介專業中心。
- AABBCC 鑑別 T1D 與 T2D(成人):Age(< 35 y 偏向 T1D)、Autoimmunity(自身或家族)、Body habitus(BMI < 25 kg/m²)、Background(家族史)、Control(noninsulin 治療無法達標)、Comorbidities(如使用 ICI)。成人新診 T1D 高達 40% 被誤診為 T2D;MODY 亦常被誤診為 T1D。
- T2D 篩檢:所有成人 35 歲開始;任何年齡 BMI ≥ 25 kg/m²(亞裔 ≥ 23 kg/m²)合併一個以上風險因子者立即篩。陰性者 ≥ 3 年複檢。糖尿病前期者每年複檢;GDM 史者終身每 1–3 年篩。
- 抗腫瘤藥誘發高血糖/糖尿病:ICI(PD-1/PD-L1,0.6–1.4% 發生率,常以 DKA 表現、需終身 insulin)、PI3Kα 抑制劑(alpelisib,grade 3–4 高血糖達 36%,中位起始 13 天)、mTOR 抑制劑(everolimus,all-grade 高血糖 27%,中位 5–6 個月)。各類用藥須在治療前、治療中以 FPG 或 random PG 監測,PI3Kα 在前 2 週每週測。
- 胰臟性糖尿病(type 3c):急性/慢性胰臟炎、胰臟切除、新生贅瘤、cystic fibrosis、hemochromatosis 等。鑑別點=同時存在 exocrine pancreatic insufficiency(fecal elastase 偏低)、影像異常、自體抗體陰性。Incretin 類藥物可能升高胰臟炎風險,應避免。急性胰臟炎後 3–6 個月與每年篩檢;慢性胰臟炎每年篩檢。
- CFRD:≥ 10 歲 cystic fibrosis 病人每年 OGTT 篩檢;OGTT 不可行時可採 A1C 兩步策略(5.5–6.4% → 進行 OGTT;≥ 6.5% 直接視為 CFRD 並確認)。CFRD 確診後 5 年起每年並行併發症監測;治療一律以 insulin。
- PTDM:移植後早期 90% 腎移植受者出現高血糖,多於出院前緩解。正式 PTDM 診斷宜於免疫抑制方案穩定(通常 3 個月)、無急性感染時以 OGTT 確立。免疫抑制方案應以個體與移植存活最佳化為主,非以 PTDM 風險決定。
- 單基因型糖尿病(< 5%):6 個月以下發病者 80–85% 為單基因型,必檢測;KCNJ11/ABCC8(neonatal diabetes)30–50% 可改用高劑量 sulfonylurea;MODY 含 14+ 基因,最常見 GCK、HNF1A、HNF4A:GCK-MODY 一般無需治療、HNF1A/HNF4A 對 sulfonylurea 反應佳;HNF1B-MODY 伴 cystic renal disease 與 hyperuricemia。
- GDM:孕前已知風險因子者孕前篩;< 15 週於首次產檢以 nonpregnant 標準篩檢未診斷糖尿病,並可篩 abnormal glucose metabolism(A1C 5.9–6.4% 或 FPG 110–125 mg/dL);24–28 週以 one-step(75-g OGTT,FPG 92/1-h 180/2-h 153 mg/dL,任一達標即診斷)或 two-step(50-g GLT → 100-g OGTT,Carpenter-Coustan 兩值達標)診斷。GDM 產後 4–12 週以 75-g OGTT 重新分類;終身每 1–3 年篩。
- One-step(IADPSG)vs. two-step:one-step 將 GDM 發生率由 5–6% 提至 15–20%;ADA 推薦 one-step,因其依妊娠終點(HAPO)建立。ACOG 仍支持 two-step,部分研究顯示兩種策略總體周產期結局無顯著差異。
摘要|Overview
- 糖尿病為一群碳水化合物代謝障礙,葡萄糖既被低效使用又因不適當的糖質新生與肝醣分解而過度產生,導致高血糖。
- 可由靜脈血漿葡萄糖升高或血液 A1C 升高診斷。
- 傳統分類:
- Type 1 diabetes(自體免疫 β 細胞破壞,多走向絕對胰島素缺乏,含 LADA)
- Type 2 diabetes(非自體免疫之 β 細胞胰島素分泌漸進性流失,常合併胰島素阻抗)
- 其他特異型糖尿病(單基因型糖尿病、外分泌胰臟疾病、藥物/化學物質誘發)
- Gestational diabetes mellitus(妊娠中後期診斷、孕前未確診者)
糖尿病診斷檢驗|DIAGNOSTIC TESTS FOR DIABETES
- 診斷依據 A1C 或血漿葡萄糖:
- FPG(fasting plasma glucose,禁食 ≥ 8 h)
- 75-g OGTT 2-h PG
- 具典型高血糖症狀(多尿、多飲、無故體重下降)或高血糖危症(DKA/HHS)時的 random plasma glucose
Recommendations|建議事項
- 2.1a 以 A1C 或血漿葡萄糖標準診斷糖尿病;血漿葡萄糖標準涵蓋 FPG、75-g OGTT 2-h PG、或合併典型高血糖症狀/高血糖危症之 random glucose(Table 2.1)。Grade B
- 2.1b 在無不模糊高血糖(如高血糖危症)時,診斷需確認檢驗(confirmatory testing)。Grade B
Table 2.1:非妊娠者糖尿病診斷標準|Criteria for the Diagnosis of Diabetes in Nonpregnant Individuals
| 標準 | 截點 |
|---|---|
| A1C | ≥ 6.5%(≥ 48 mmol/mol)。應採 NGSP 認證、追溯至 DCCT 之方法。* |
| FPG | ≥ 126 mg/dL(≥ 7.0 mmol/L)。禁食定義為 ≥ 8 h 無熱量攝取。* |
| 75-g OGTT 2-h PG | ≥ 200 mg/dL(≥ 11.1 mmol/L)。OGTT 須依 WHO 規範以含 75 g 無水葡萄糖溶於水的負荷量。* |
| Random PG | 具典型高血糖症狀或高血糖危症時 ≥ 200 mg/dL(≥ 11.1 mmol/L),不限與餐後時間。 |
[!tip]- Table 2.1 讀表教學
- 「*」表在無不模糊高血糖時,診斷需兩次異常結果(同次抽血做兩項不同檢驗,例如 A1C + FPG;或同一檢驗相隔不同時間複測)。
- 缺寫:DCCT=Diabetes Control and Complications Trial;NGSP=National Glycohemoglobin Standardization Program;FPG=fasting plasma glucose;OGTT=oral glucose tolerance test;2-h PG=2-h plasma glucose。
- Random PG 路徑必須伴隨「典型症狀/高血糖危症」之臨床情境,否則須回到三項實驗室路徑。
檢驗一致性與偏好|Screening and Diagnosis of Diabetes
- 三項檢驗反映不同葡萄糖代謝面向,截點識別出之族群不完全重疊。
- 與 FPG 與 A1C 截點相比,2-h PG 可診斷出更多 prediabetes 與 diabetes。
- T2D 一級預防(即防止 prediabetes 進展為 T2D)證據主要來自具 IGT(合併或不合併 IFG 升高)者。
- 對單獨 IFG 或單獨以 A1C 定義之 prediabetes 之預防效益不確定。
- 同一組檢驗可同時用於篩檢、診斷糖尿病與 prediabetes(Table 2.1 與 Table 2.2)。
- 糖尿病可在多種臨床情境下被識別:
- 看似低風險者偶然測得葡萄糖
- 依風險評估而篩檢者
- 已有高血糖症狀或徵象者
- 目前證據不足支持以 CGM(continuous glucose monitoring)作為 prediabetes 或糖尿病篩檢/診斷工具。
Table 2.2:非妊娠者糖尿病前期定義|Criteria Defining Prediabetes in Nonpregnant Individuals
| 標準 | 範圍 |
|---|---|
| A1C | 5.7–6.4%(39–47 mmol/mol) |
| FPG(IFG) | 100 mg/dL(5.6 mmol/L)至 125 mg/dL(6.9 mmol/L) |
| 2-h PG during 75-g OGTT(IGT) | 140 mg/dL(7.8 mmol/L)至 199 mg/dL(11.0 mmol/L) |
[!tip]- Table 2.2 讀表教學
- 三項標準對應風險為連續性(低於下限仍存在風險,越接近上限風險越高)。
- 三項並非全等價:建議介入策略與證據基礎主要建立於 IGT 族群。
- WHO 與部分機構仍維持 IFG 下限為 110 mg/dL(6.1 mmol/L);ADA 1997 採 110,2003 改為 100,使具 IFG 風險族群與具 IGT 族群可比。
以 FPG 或 2-h PG 篩檢與診斷糖尿病|Use of Fasting Plasma Glucose or 2-Hour Plasma Glucose
- 具典型高血糖症狀或高血糖危症時,random plasma glucose 即足以診斷糖尿病(症狀/危症 + random PG ≥ 200 mg/dL)。
- 此時血糖數值除確認症狀來源外,亦會引導治療決策。
- 同時測 A1C 有助判斷高血糖慢性程度。
- 無症狀者:以 FPG 或 2-h PG 篩檢與診斷。
- 非妊娠者通常以 FPG(或 A1C)為例行篩檢首選(操作簡便)。
- 75-g OGTT 敏感度顯著高於前兩者,特定情境(cystic fibrosis–related diabetes、posttransplantation diabetes mellitus)優先建議使用。
- 缺典型症狀時,無論用何檢驗皆需重複測試確認診斷(見「Confirming the Diagnosis」)。
- 葡萄糖檢驗的優缺點:
- 優:低成本、廣泛可得。
- 缺:日內變異大、需禁食 ≥ 8 h;近期運動/疾病/急性壓力影響濃度;糖解作用(glycolysis)可使未即時處理之檢體偽低。
- OGTT 前 3 日須維持混合飲食且每日 ≥ 150 g 碳水。
- 事前限制碳水會偽升 postchallenge 葡萄糖 → 可能偽陽。
以 A1C 篩檢與診斷糖尿病|Use of A1C for Screening and Diagnosis of Diabetes
Recommendations|建議事項
- 2.2a A1C 須採 NGSP 認證、追溯至 DCCT 之方法。Grade B
- 2.2b Point-of-care A1C 用於糖尿病篩檢/診斷僅限 FDA 核准診斷用途之機型,且於 CLIA 認證、由訓練人員執行 moderate complexity 以上檢驗之實驗室。Grade B
- 2.3 當血糖值與 A1C 結果之間出現一致且顯著的不一致時,評估兩項檢驗有無問題或干擾。Grade B
- 2.4 若處於改變 A1C 與血糖關係之狀況(部分 hemoglobin variants、妊娠、G6PD 缺乏、HIV、改變紅血球生命週期之疾病),改以血漿葡萄糖標準診斷糖尿病。Grade B
Table 2.3:葡萄糖與 A1C 實驗室檢驗的考量與解讀|Considerations Related to the Use and Interpretation of Laboratory Measurements of Glucose and A1C
| 項目 | Glucose | A1C |
|---|---|---|
| 成本 | 便宜,全球大多實驗室可取得 | 較貴,全球可得性較低 |
| 高血糖時相 | 急性測量 | 慢性測量(涵蓋過去約 2–3 個月) |
| 預分析穩定度 | 差;血漿須立即分離或檢體置於冰上以防糖解 | 佳 |
| 檢體 | 因檢體型態(plasma/serum/whole blood)與來源(capillary/venous/arterial)而異 | 需 whole-blood |
| 檢驗標準化 | 未標準化 | 已良好標準化 |
| 禁食 | 需禁食或定時抽血 | 非禁食檢驗,無需準備 |
| 個體變異 | 高 | 低 |
| 急性影響因子 | 進食、壓力、近期疾病、活動 | 不受近期進食、壓力、疾病、活動影響 |
| 其他個體影響因子 | 日夜變異、藥物、酒精、吸菸、bilirubin | 紅血球更新異常(貧血、鐵狀態、脾切除、出血、輸血、溶血、G6PD 缺乏、erythropoietin)、HIV、cirrhosis、kidney failure、dialysis、妊娠 |
| 檢驗干擾 | 視 assay:檢體處理時間、溶血、嚴重高三酸甘油酯、嚴重高 bilirubin | 視 assay:hemoglobin variants、嚴重高三酸甘油酯、嚴重高 bilirubin |
[!tip]- Table 2.3 讀表教學
- 雙欄並列:左欄 Glucose 強項是「即時、便宜、廣泛」;右欄 A1C 強項是「免禁食、穩定、標準化」。
- 任何改變紅血球生命週期或 hemoglobin 結構的狀況都應將判讀重心轉回血糖標準。
- 若同一個體血糖與 A1C 持續顯著不一致,須懷疑分析問題或干擾,並評估其臨床意涵;可改以 fructosamine 或 glycated albumin 監測。
A1C 檢驗運作與限制
- 應採 NGSP 認證、追溯/標準化至 DCCT 之方法(ngsp.org)。
- 美國以外多數採 IFCC 認證(同等嚴謹流程)。
- POC A1C 機型可能 NGSP 認證並 FDA 核可用於糖尿病管理監測,於 CLIA 認證或 CLIA-waived 場域使用。
- 用於診斷需 FDA 核准診斷用途之機型,且於 CLIA 認證實驗室;包含人員資格(含每年能力評估)與每年三次以上參與認可的能力測試計畫。
- A1C 相對 FPG/OGTT 的優點:
- 免禁食
- 預分析穩定度佳
- 對壓力、營養變化、疾病的日間擾動較小
- 限制:
- 在指定截點處的敏感度低於 2-h PG
- 部分區域可得性受限
- 為間接量度;任何影響 hemoglobin 濃度或紅血球更新的因素皆會影響 A1C
- A1C 反映 erythrocyte 生命週期(約 120 天)內葡萄糖與 hemoglobin 結合,為「加權」平均,近期血糖暴露權重較高。
- 臨床上有意義的 A1C 變化可在 < 120 天內出現。
- 不適用 A1C 之族群:
- Anemia、erythropoietin 治療中、血液透析、HIV 治療
- Thalassemia、folate 缺乏
- Hemoglobin variants 干擾:
- Sickle cell trait 須選擇不受 variant 干擾之 assay。
- 干擾清單見 ngsp.org/interf.asp。
- G6PD G202A(X-linked,美國黑人 11% 帶有):
- 同合子男性 A1C 約低 0.8%,同合子女性低約 0.7%。
- A1C 種族差異:
- 黑人 A1C 較非西班牙裔白人或西班牙裔約高 0.3%。
- 不應以 race/ancestry 作為基因差異之代用變項。
- A1C 與併發症風險的關聯在黑人與非西班牙裔白人族群相似。
Confirming the Diagnosis|診斷確認
- 在無明確臨床診斷(如典型症狀/高血糖危症 + random PG ≥ 200 mg/dL)時,需 confirmatory tests 確立診斷。
- 兩種完成方式:
- 同次抽血以兩項異常檢驗結果(如 A1C + FPG 同時達標)
- 兩個不同時間點的異常結果(同檢驗複測或不同檢驗)
- 範例:
- A1C 7.0%(53 mmol/mol),複測 6.8%(51 mmol/mol) → 確診糖尿病。
- 兩種不同檢驗(如 A1C + FPG)同時達截點 → 確診。
- 不一致結果處理:
- 將達截點的那項檢驗複測,並考量影響 A1C 或血糖之因素。
- 例:若達 A1C 截點(兩次 ≥ 6.5%)但 FPG 未達(< 126 mg/dL)→ 仍視為糖尿病。
- 接近截點之結果:
- 教育個案高血糖症狀,3–6 個月後複檢。
- 持續且顯著的血糖/A1C 不一致:
- 追查潛在原因(含分析問題或干擾)與臨床意涵。
- 監測糖尿病者糖化指標可改用 fructosamine 或 glycated albumin。
分類|CLASSIFICATION
Recommendation|建議事項
- 2.5 將高血糖個案分入適當診斷類別,以利個人化處置。Grade E
分類框架
- 傳統分為四類,但正在依基因、metabolomic、其他特徵與病理生理重新審視:
- Type 1 diabetes(自體免疫 β 細胞破壞,通常導致絕對胰島素缺乏,包含 LADA)
- Type 2 diabetes(非自體免疫之 β 細胞胰島素分泌漸進性流失,常合併胰島素阻抗)
- 其他特異型糖尿病(單基因型糖尿病、外分泌胰臟疾病、藥物/化學物誘發)
- Gestational diabetes mellitus(妊娠中後期診斷、孕前未明顯糖尿病;亦含妊娠中其他型糖尿病如 T1D)
異質性與分類落差
- T1D/T2D 為異質性疾病,臨床表現與進展差異大。
- 分類用於個人化治療,但部分個案於診斷時無法明確歸類。
- 「T2D 僅成人發生、T1D 僅兒童發生」為過時典範:兩型皆可發生於各年齡層。
- T1D 兒童常以多尿/多飲表現,約半數以 DKA 起病。
- 成人 T1D 起病較多變:可能無典型兒童症狀、insulin 替代之進展較緩慢。
- 最具辨別力的 T1D 特徵:
- 較年輕發病(< 35 歲)
- 較低 BMI(< 25 kg/m²)
- 無故體重下降
- 酮酸中毒
- 起病時 plasma glucose > 360 mg/dL(> 20 mmol/L)
- 非典型情境:
- T2D 偶以 DKA 表現(ketosis-prone diabetes,常見於黑人、西班牙/拉丁裔);早期需 insulin 治療通常為暫時性。
- 成人新診 T1D 高達 40% 被誤診為 T2D;MODY 常被誤診為 T1D。
- AABBCC 鑑別工具(協助辨別 T1D 與 T2D,未經前瞻驗證):
- Age:< 35 歲考慮 T1D
- Autoimmunity:個人或家族自體免疫疾病、polyglandular autoimmune syndrome
- Body habitus:BMI < 25 kg/m²
- Background:T1D 家族史
- Control(建議改稱「goal」):noninsulin 治療無法達血糖目標
- Comorbidities:例如 ICI 抗腫瘤治療可引發急性自體免疫糖尿病
共病與重疊
- T1D/T2D 皆為遺傳與環境因素導致 β 細胞質量/功能漸進性流失,臨床表現為高血糖。
- 高血糖出現後,所有型糖尿病皆有相似慢性併發症風險,僅進展速率不同。
- T1D 不排斥同時具備 T2D 典型特徵(胰島素阻抗、肥胖、其他代謝異常)。
- 在更精確分群進入臨床前,可標記為兩型特徵兼備,以利取得 CGM 與適當治療(如 GLP-1 RA 或 SGLT2i 之體重與心代謝益處)。
T1D 病理生理進展
- 持續存在兩個以上 islet 自體抗體幾乎可預測臨床糖尿病。
- 從出生或幼年追蹤的高風險世代:
- 6 月齡前血清轉陽罕見
- 9–24 月齡為轉陽高峰
- 從 preclinical 到 symptomatic 進展速率取決於:
- 首次抗體偵測年齡
- 抗體數
- 抗體特異性
- 抗體效價
- 葡萄糖與 A1C 可能在臨床發病前升高(FPG/2-h PG 約於診斷前 6 個月即可變化)。
- T1D 三階段架構(Table 2.4)作為研究與監管決策框架。
對於 LADA 命名的爭議
- 是否將緩進性自體免疫成人糖尿病稱 LADA 或視為 T1D 仍有爭議。
- 本指引將「自體免疫 β 細胞破壞所致」之糖尿病一律歸入 T1D,不論發病年齡。
- LADA 一詞在臨床仍常用且可接受,提醒臨床醫師留意成人緩進性自體免疫破壞,以加速 insulin 啟用、避免血糖惡化或 DKA。
- 仰賴未經驗證之自體抗體檢驗會將部分 T2D 誤分為 LADA;應採高特異性檢驗、確認其他自體抗體並限於具自體免疫糖尿病臨床特徵者。
T2D 病理生理
- T2D 之 β 細胞破壞與功能異常路徑更為異質,但「不足之 β 細胞 insulin 分泌與 β 細胞功能異常」(常於胰島素阻抗背景下)為共同特徵。
- T2D 之 insulin 分泌缺陷與遺傳易感、表觀遺傳改變、發炎、代謝壓力相關。
- 未來分類將以 β 細胞功能異常之病理生理為核心。
Table 2.4:T1D 分期|Staging of Type 1 Diabetes
| 項目 | Stage 1 | Stage 2 | Stage 3 |
|---|---|---|---|
| 特徵 | 自體免疫;正常血糖;無症狀 | 自體免疫;血糖異常(dysglycemia);無症狀 | 自體免疫;顯性高血糖;有症狀 |
| 診斷標準 | 多個 islet 自體抗體;無 IGT/IFG,A1C 正常 | islet 自體抗體(通常多個);血糖異常:IFG(FPG 100–125 mg/dL)、IGT(2-h PG 140–199 mg/dL)、A1C 5.7–6.4%(39–47 mmol/mol)或 A1C 增加 ≥ 10% | 自體抗體可能消失;達標準糖尿病診斷 |
[!tip]- Table 2.4 讀表教學
- 三階段對應「免疫先行 → 代謝失衡 → 顯性疾病」。
- 替代 Stage 2 標準:OGTT 30、60、90 分血糖 ≥ 200 mg/dL(≥ 11.1 mmol/L)並於 ≥ 18 歲者進行確認檢驗(已用於臨床試驗)。
- dysglycemia 可由表中任一條件定義,不需全數符合。
- Stage 3 自體抗體可能轉陰,故臨床表現與血糖達標準是診斷重心。
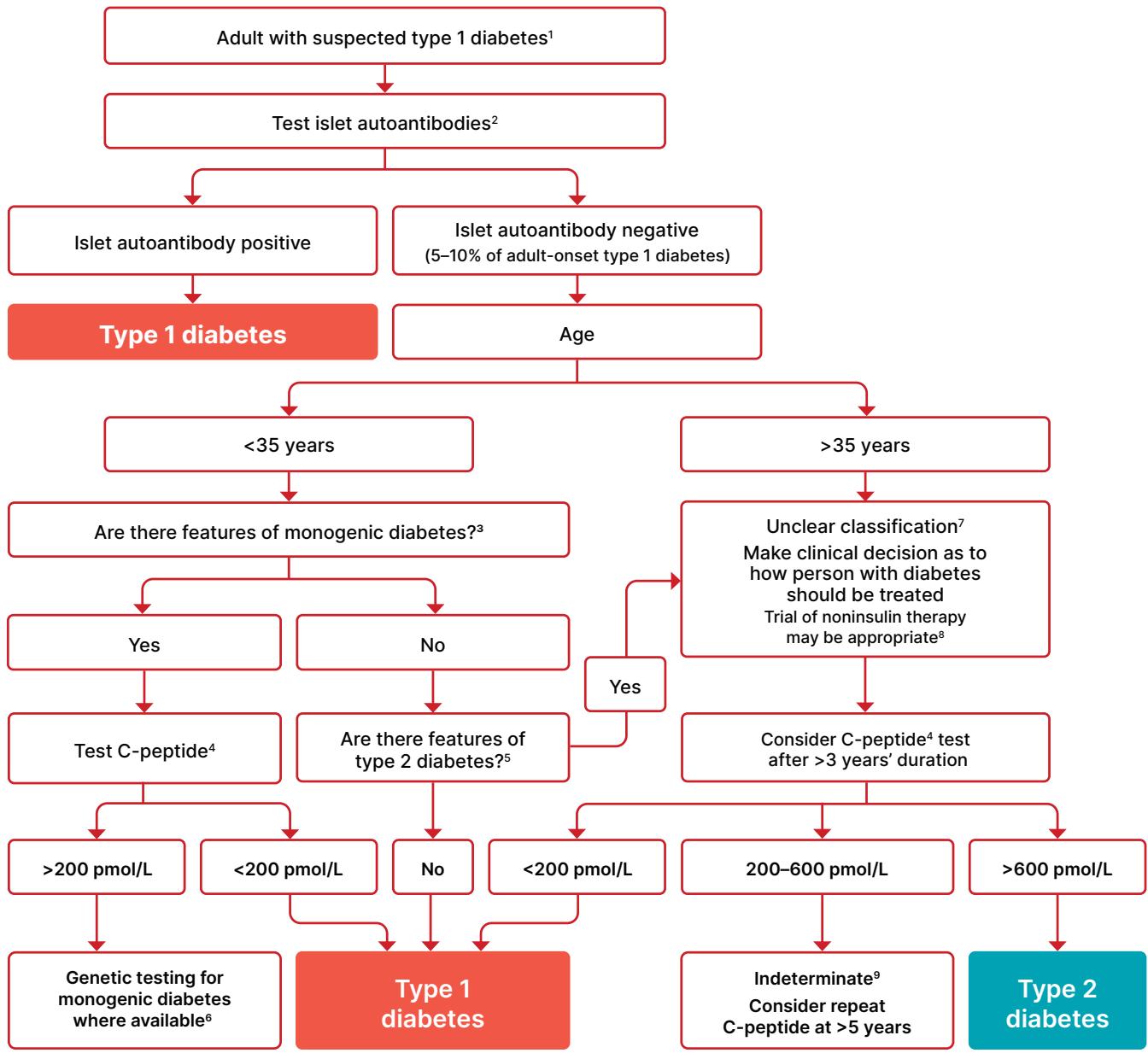
Figure 2.1(白人歐洲族群資料推導):成人疑似 T1D 之分類流程圖。
- 沒有單一臨床特徵可獨立確診 T1D。
- 自體抗體檢測首選 GAD;陰性時依序加測 IA-2、ZnT8;未接受 insulin 者可加測 anti-insulin antibody。
- 35 歲以下、無 T2D/單基因型臨床特徵者,自體抗體陰性不改變 T1D 診斷(5–10% T1D 無抗體)。
- 單基因型糖尿病線索:診斷時 A1C < 7.5%(< 58 mmol/mol)、單側父母糖尿病、特殊單基因型徵象(renal cyst、partial lipodystrophy、母系遺傳耳聾、無肥胖之嚴重胰島素阻抗)、ModyCalculator 機率 > 25%。
- C-peptide 僅在已使用 insulin 者測;進食後 5 h 內 random C-peptide(同步 glucose)可取代正式 stimulation;≥ 600 pmol/L(≥ 1.8 ng/mL)情境不影響判讀;< 600 pmol/L 且同步 glucose < 70 mg/dL 或可能禁食時應重測;< 80 pmol/L(< 0.24 ng/mL)無需重測。
- C-peptide 測量須在停 insulin 前進行以排除嚴重 insulin 缺乏;高血糖危症後 2 週內勿測。
- T2D 線索:BMI ≥ 25 kg/m²、無體重下降、無酮酸中毒、高血糖較輕。
- 若基因檢測未確認單基因型 → 分類不明,依臨床判斷治療。
- 較年長者強烈考慮 T2D,部分需考慮 pancreatic 或其他型糖尿病。
- 疑似 T1D 但未用 insulin 者須密切監測與衛教,血糖惡化時迅速啟用 insulin。
- C-peptide 200–600 pmol/L(0.6–1.8 ng/mL)通常符合 T1D 或 MODY,亦可見於 BMI 正常/低或長病程之 insulin-treated T2D。
TYPE 1 DIABETES
Recommendations|建議事項
- 2.6 以 IA、GAD、IA-2 或 ZnT8 自體抗體篩檢 presymptomatic T1D。Grade B
- 2.7 自體抗體篩檢應提供給 T1D 家族史或已知具高遺傳風險者。Grade B
- 2.8a 篩檢結果一個以上 islet 自體抗體陽性者,應評估是否已達 stage 3(顯性 T1D)(A1C、urinalysis 與/或血漿葡萄糖),需立即臨床處置與衛教。Grade B
- 2.8b 多項 islet 自體抗體確認陽性且無顯性 T1D 者,進展至 stage 3 風險高,應轉介專業中心進行代謝分期(Table 2.4)、衛教,並評估參加預防性試驗或核可治療(如 teplizumab)。Grade B
- 2.9 單一 IA-2 自體抗體確認陽性者應比照多抗體陽性者監測,因 IA-2 為獨立進展風險因子。Grade B;單一 islet 自體抗體陽性者依年齡每 6 個月至 3 年複測抗體,評估持續性或血清轉換。Grade E
- 2.10 對於具與 T1D 重疊之表型風險因子之成人(年輕、無故體重下降、酮酸中毒、短時間內需 insulin),建議進行標準化 islet 自體抗體檢測以分類糖尿病。Grade E
Immune-Mediated Diabetes|免疫介導型糖尿病
- 自體免疫 T1D 占糖尿病 5–10%,由胰臟 β 細胞自體免疫破壞引起。
- 自體免疫標記:
- islet cell 自體抗體
- GAD(GAD65)自體抗體
- insulin autoantibody
- IA-2、IA-2β(tyrosine phosphatase)自體抗體
- ZnT8 自體抗體
- 預防/延遲 T1D 之臨床試驗持續進行(trialnet.org)。
- 強烈 HLA 關聯:
- 連結 DQB1 與 DRB1 haplotype。
- 易感 alleles:DRB1*0301-DQB1*0201(DR3-DQ2)、DRB1*0401-DQB1*0302(DR4-DQ8)。
- 保護 alleles:DRB1*1501、DQA1*0102-DQB1*0602。
- T1D 階段:
- Stage 1:兩個以上自體抗體 + 正常血糖;5 年發展為症狀 T1D 風險約 44%(依抗體數、效價、特異性、血清轉換年齡與遺傳風險變異甚大)。
- Stage 2:islet 自體抗體(通常多個)+ 未達糖尿病之 dysglycemia(依 Table 2.4 任一條件);進展至 stage 3 之 2 年風險約 60%、5 年風險約 75%。
- 一個以上 islet 自體抗體陽性者,應立即進行 stage 3 早期診斷檢驗,以避免轉介等待造成的延誤。
- 早期辨識顯性高血糖可預防 stage 3 起病時 DKA、引導轉介急迫性。
- Diabetes Prevention Trial-Type 1 顯示半年一次 OGTT 之高風險家族成員,發病時 DKA 風險僅 4%(相對未進入監測者顯著降低)。
- 抗體追蹤頻率(Phillip 共識報告):
- 單一抗體陽性者需代謝評估(部分個案會於接近 stage 3 時失抗體)。
- 單一 IA-2 抗體陽性者,與多抗體陽性者風險相當,須等同密切監測。
- 單一非 IA-2 抗體:進展風險異質,依年齡、抗體型態、其他風險而定。
- 兒童族群數據:
- 持續單一 islet 自體抗體者,10 年累積進展至臨床 T1D 約 14–15%。
- 多數風險於血清轉換後 2 年內累積。
- 風險最高者:年幼、單一 IA-2 抗體陽性。
- 成人風險較低且隨年齡降低;最佳追蹤頻率資料有限,依兒童模式與專家經驗外推。
- 實務追蹤頻率:
- 抗體面板:GAD、IA-2、insulin、ZnT8 + 一次 random venous/capillary glucose + A1C
- ≤ 3 歲:每 6 個月一次共 3 年,再每年一次共 3 年
- 3–18 歲:每年一次;3 年無進展可考慮停止
- 成人:每 3 年一次;具額外風險(其他自體免疫疾病、高遺傳風險評分、一等親 T1D)者每年一次
- Stage 3 成人 T1D:
- 單獨 GAD 抗體陽性常見,與內生 insulin 流失較緩相關。
- T1D 早期單一 GAD65 抗體陽性與 stage 3 進展較緩相關(相較 IA-2 或 ZnT8)。
β 細胞破壞速率
- 個體差異大;嬰幼兒/兒童多為快速,成人多為緩慢(並非絕對)。
- 兒童/青少年常以 DKA 為首發表現,美國 20 年來 DKA 發生率上升。
- 部分個案僅輕度禁食高血糖,於感染或其他壓力下迅速轉為嚴重高血糖/DKA。
- 成人可保留足夠 β 細胞功能多年,遲早變為 insulin dependent 並承擔 DKA 風險。
- 後期幾近無 insulin 分泌(plasma C-peptide 低或測不到)。
- 自體免疫 β 細胞破壞具多重遺傳因子與環境因素。
- 起病時無肥胖為傳統印象,但隨一般肥胖人口上升,肥胖不應排除 T1D 檢驗。
- T1D 易合併其他自體免疫疾病:Hashimoto 甲狀腺炎、Graves disease、celiac disease、Addison disease、vitiligo、自體免疫肝炎、myasthenia gravis、pernicious anemia。
- 單基因 polyglandular autoimmune syndromes:
- IPEX:FOXP3 基因突變,X-linked。
- AIRE 基因突變所致疾病。
病毒與感染相關性
- 與 T1D 關聯之病毒:enterovirus(如 Coxsackievirus B)。
- COVID-19 早期報告:高血糖、DKA、新發 T1D 增加,懷疑 SARS-CoV-2 為觸發或加速者。
- 後續大型 cohort 與註冊研究結果不一:
- 部分顯示 COVID-19 後 T1D 風險小幅升高。
- 部分歸因於就醫障礙與診斷延遲。
- 提示初期觀察可能反映病毒效應與間接 pandemic 因素並存;CoviDIAB Registry 持續追蹤長期關係。
免疫檢查點抑制劑誘發之自體免疫糖尿病|Immune Checkpoint Inhibitor–Induced Autoimmune Diabetes
- ICI(cancer immunotherapy)可引發免疫系統活化、產生自體免疫疾病。
- 表現:
- 自體免疫糖尿病可呈 fulminant(猛爆)發病、伴 DKA、低或測不到 C-peptide。
- 不到一半個案有 islet 自體抗體;多數無 partial remission(與典型 T1D 不同)。
- 提示部分病理生理與 T1D 不同。
- 流行病學:
- 0.6–1.4% 接受 ICI 者發生。
- PD-1/PD-L1 抑制劑(單用或合併 anti-CTLA-4)較常見。
- HLA 與遺傳:
- 多數案例帶 T1D 高風險 HLA haplotype。
- 中性或保護性 haplotype 仍可能發生。
- 臨床意涵:
- 風險目前無法以家族史或抗體預測。
- 投藥/照護人員應警覺、衛教與監測。
Idiopathic Type 1 Diabetes|原發型 T1D
- 部分 T1D 無已知病因。
- 永久 insulinopenia、易發 DKA、無 β 細胞自體免疫證據。
- 僅少數 T1D 屬此類。
T1D 篩檢|Screening for Type 1 Diabetes Risk
- T1D 發生率與盛行率持續上升。
- 起病常以急性高血糖與顯著高糖表現;25–50% 以致命 DKA 起病。
- 約 90% 新診 T1D 無已知罹 T1D 親屬。
- 多項研究顯示,量測 T1D 親屬、一般兒童族群、或具高遺傳風險兒童的 islet 自體抗體可識別未來發病者。
- Finland/Germany/U.S. 三 cohort 共 585 名兒童:
- 出現兩個以上抗體後 10 年內進展至 T1D 約 70%、15 年 84%。
- Finland 與美國組為一般族群,德國組為 T1D 父母後代;三組結果一致 → 散發型與家族型 T1D 進展機制相同。
- 抗體數量與風險呈正比。
- TEDDY study:3 歲時具 ≥ 1 抗體之 363 名兒童,21% 發展為 T1D。
- 抗體檢驗 + 衛教 + 密切追蹤:可使早期診斷、預防 DKA。
- 有 50% 兒童僅單一抗體者於追蹤中轉陰 → 首次陽性應於 3 個月內以第二次檢驗確認,建議使用符合 IASP 標準之實驗室。
- T1D 遺傳風險評分:
- 已用於新生兒篩檢以辨識未來發病風險。
- 模擬研究:> 77% 將發病者可在一般族群 10% 內被找出 → 可作為抗體檢驗最受益對象。
- 既有研究多為歐裔;其他族裔差異化能力仍待大規模 case-control 驗證。
- 篩檢計畫:
- 歐洲:Fr1da、gppad.org
- 澳洲:type1screen.org
- 美國:trialnet.org、askhealth.org、cascadekids.org
- 一般族群篩檢適用於高品質檢驗與後續資源具備地區。
- Italy 2023 起對 1–17 歲全國推行 T1D 與 celiac 篩檢。
- 抗體陽性者應提供/轉介糖尿病風險、症狀與 DKA 預防諮詢,並考慮專業中心進一步評估、臨床試驗或核可治療(延緩臨床糖尿病)。
PREDIABETES AND TYPE 2 DIABETES
Recommendations|建議事項
- 2.11 以風險因子評估或經驗證之風險計算器篩檢無症狀成人之 prediabetes 與 T2D 風險。Grade B
- 2.12a 任何年齡、過重或肥胖且具一個以上風險因子(Table 2.5)之成人應考慮 prediabetes 或 T2D 檢驗。Grade B
- 2.12b 其他成人於 35 歲開始篩檢。Grade B
- 2.12c 篩檢無 prediabetes 或糖尿病者,至少每 3 年複檢;具症狀或風險改變(如體重增加)時提早。Grade C
- 2.13 篩檢工具:FPG、75-g OGTT 2-h PG、A1C 皆適用。Grade B
- 2.14 以 OGTT 篩檢時,前 3 日須 ≥ 150 g/day 碳水。Grade C
- 2.15 兒童/青少年於青春期或 ≥ 10 歲(兩者較早者)開始基於風險之篩檢,條件為:BMI ≥ 85 百分位(過重)或 ≥ 95 百分位(肥胖)併具一個以上風險因子(Table 2.6)。Grade B
- 2.16a 服用特定藥物(statins、thiazide 利尿劑、部分 HIV 藥物)者考慮篩檢 prediabetes 或糖尿病。Grade C
- 2.16b 服用第二代抗精神病藥物者,於起始時、起始後 12–16 週(必要時更早)、之後每年篩檢。Grade B
- 2.17 HIV 個案於起始 ARV 前、轉換 ARV 時、起始或轉換後 3–6 個月以 FPG 篩檢糖尿病與 prediabetes;初次正常者每年 FPG 一次。Grade E
- 2.18 反覆或長期使用 glucocorticoids 者監測餐後或 random glucose。Grade B
Table 2.5:無症狀成人糖尿病/糖尿病前期篩檢標準
- 過重或肥胖(BMI ≥ 25 kg/m² 或亞裔 ≥ 23 kg/m²)成人併下列一個以上風險因子者考慮篩檢:
- 一等親糖尿病
- 高風險族裔(非裔美國人、拉丁裔、原住民、亞裔美國人)
- 心血管疾病史
- 高血壓(≥ 130/80 mmHg 或正在治療)
- HDL 膽固醇 < 35 mg/dL(< 0.9 mmol/L)和/或三酸甘油酯 > 250 mg/dL(> 2.8 mmol/L)
- 多囊性卵巢症候群
- 缺乏身體活動
- 其他與胰島素阻抗相關的臨床狀況(嚴重肥胖、acanthosis nigricans、metabolic dysfunction-associated steatotic liver disease)
- Prediabetes(A1C ≥ 5.7%、IGT 或 IFG)者每年檢驗。
- GDM 史者至少每 1–3 年檢驗。
- 其他人於 35 歲開始檢驗。
- 結果正常者至少每 3 年複檢;視初檢結果與風險可更頻繁。
- 其他高風險族群(HIV、暴露於高風險藥物、牙周病、胰臟炎史)亦須密切監測。
[!tip]- Table 2.5 讀表教學
- 1 與 4 為入口策略:年齡分流(35 歲)+ BMI + 至少一項風險因子。
- 2、3、6 為「已知高風險」之追蹤頻率調整。
- 亞裔 BMI 截點獨立提前至 23 kg/m²,反映內臟脂肪比例差異。
- 心血管/代謝項(高血壓、血脂異常、PCOS、MASLD)皆為共病提示。
Table 2.6:兒童/青少年無症狀者糖尿病前期或 T2D 風險篩檢
於青春期或 ≥ 10 歲(兩者較早者)後,過重(≥ 85 百分位)或肥胖(≥ 95 百分位)兒童/青少年併下列一個以上風險因子者考慮篩檢:
- 母親糖尿病或妊娠期 GDM 史 — Grade A
- 一等或二等親 T2D 家族史 — Grade A
- 高風險族裔(見 Table 2.5)— Grade A
- 胰島素阻抗徵象或相關狀況(acanthosis nigricans、高血壓、血脂異常、PCOS、large/small-for-gestational-age 出生體重)— Grade B
[!tip]- Table 2.6 讀表教學
- 兒童篩檢入口同時要求年齡(青春期或 ≥ 10 歲)、體位(過重/肥胖)、與一個以上風險因子。
- 結果正常者至少每 3 年複檢,BMI 上升或風險惡化時可更頻繁。
- 10 歲以下 T2D 病例存在;具多項風險因子可考慮提前。
Prediabetes|糖尿病前期
- 為血糖/A1C 介於正常與糖尿病之間的中間範圍。
- 定義:IFG 與/或 IGT 與/或 A1C 5.7–6.4%(39–47 mmol/mol)(Table 2.2)。
- 為糖尿病、心血管疾病與多項心代謝結果之顯著風險因子。
- 與肥胖(尤其腹部/內臟)、血脂異常(高三酸甘油酯/低 HDL)、高血壓相關。
- 出現 prediabetes 應綜合篩檢心血管風險因子。
Diagnosis of Prediabetes|糖尿病前期診斷
- IFG:FPG 100–125 mg/dL(5.6–6.9 mmol/L)。
- WHO 與部分組織 IFG 下限為 110 mg/dL;ADA 1997 採 110,2003 改為 100,使具 IFG 風險族群與 IGT 族群可比。
- IGT:75-g OGTT 2-h PG 140–199 mg/dL(7.8–11.0 mmol/L)。
- A1C 連續關聯:
- 系統回顧 16 cohort(44,203 人,平均追蹤 5.6 年):A1C 5.5–6.0%(37–42 mmol/mol)5 年發病率 9–25%;6.0–6.5%(42–48 mmol/mol)5 年發病率 25–50%(相對 A1C 5.0% 之相對風險約 20 倍)。
- 黑人與非西班牙裔白人社區研究:基線 A1C 為糖尿病與 CV 事件較強預測指標(強於 fasting glucose)。
- DPP 中基線 A1C 亦為發展為葡萄糖標準糖尿病的強預測指標。
- A1C 5.7–6.4%(39–47 mmol/mol)為高風險族群:
- 應告知 CV 與糖尿病風險、提供有效降風險策略。
- 連續性、曲線形:A1C 上升、糖尿病風險不成比例上升。
- 極高風險者(A1C > 6.0%、IFG + IGT 並存)應採積極介入與密切追蹤。
- ADA 風險測試(diabetes.org/diabetes-risk-test)為民眾與專業人員的篩檢適用性評估工具。
Type 2 Diabetes|第 2 型糖尿病
- 占糖尿病 90–95%。
- 多以相對(非絕對)insulin 缺乏與 insulin 阻抗為特徵。
- 異質性受到日益重視。
- 多數 T2D 過重或肥胖,但即使 BMI 正常者亦可能具腹部脂肪堆積(含 MASLD 與 ectopic 部位如骨骼肌)。
- 急症:
- 自發性 DKA 在 T2D 罕見,但相對 insulinopenia 加上誘發因子(其他疾病壓力如 COVID-19 或心肌梗塞、毒品、藥物如 glucocorticoids/SGLT2 抑制劑)可發生。
- HHS 多與 T2D 相關(既存或新診),以嚴重高血糖、高滲、脫水為特徵,無顯著酮酸中毒。
- 可同時具 DKA 與 HHS 混合表現。
- T2D 常多年未診:高血糖漸進,早期可能無典型症狀(視力模糊、脫水、體重下降)。
- 未診者承受不同程度未治療高血糖 → 微/巨血管併發症風險上升。
- 病理生理:
- 初期可有正常或升高之 insulin 濃度,但無法正常化血糖代表「葡萄糖刺激下 insulin 分泌相對不足」以代償阻抗。
- 阻抗可由減重、運動、藥物治療改善,但少能完全恢復。
- Intensive lifestyle interventions 與/或 metabolic surgery 可帶來糖尿病緩解。
- 風險因子:
- 年齡、肥胖、缺乏身體活動。
- 在 prediabetes、GDM 史、PCOS 者更頻繁。
- 高血壓、血脂異常、特定族裔。
- 部分藥物(如 glucocorticoids)為顯著風險因子。
- 鑑別:成人具非典型風險或年齡較輕者,考慮 islet 抗體檢驗排除 T1D。
無症狀成人之 prediabetes/T2D 篩檢|Screening and Testing for Prediabetes and Type 2 Diabetes in Asymptomatic Adults
- 以風險因子評估(Table 2.5)或 ADA 風險測試為入口指引臨床醫師決定是否進行診斷檢驗。
- 兩者皆符合「篩檢條件」:常見、長 presymptomatic 期、簡易檢驗可得、糖期負擔為強預後因子。
- 介入策略應個別化、評估風險效益比與個案目標。
- 風險模型:高風險者介入受益最大。
- DPPOS:預防 prediabetes → 糖尿病進展可降低 retinopathy 與 nephropathy 發生率。
- 美國/全球許多人仍未診或於併發症出現後才診。
年齡|Age
- 為糖尿病主要風險因子。
- 不晚於 35 歲開始篩檢。
- 任何年齡過重或肥胖併一個以上風險因子者考慮篩檢。
藥物|Medications
- 應篩檢服用下列藥物者:glucocorticoids、statins、thiazide 利尿劑、部分 HIV 藥物、第二代抗精神病藥物。
- 機制多為促進胰島素阻抗。
- Glucocorticoid 引發糖尿病:
- 用於自體免疫病、免疫抑制(移植)、抗腫瘤輔助治療等。
- 盛行率與藥物半衰期、劑量、頻率、療程相關。
- 風險因子(肥胖)或合用其他藥物(tacrolimus)會加重。
- 高劑量(≥ 5 mg prednisolone 或等效)下發生率 18–32%。
- 篩檢/衛教不一致。
- 應以餐後(餐後 1–2 h)或 random glucose 篩檢,而非禁食(glucocorticoid 誘發者多為阻抗為主,FPG 易低估)。
- 門診實務:每週 2 次測糖;≥ 200 mg/dL 改為每日。
- 抗腫瘤情境:每日 capillary glucose 監測,連續兩次 ≥ 220 mg/dL 立即治療。
- 第二代抗精神病藥物:
- 與 T2D 風險升高相關,常合併血脂異常與體重增加。
- 起始時、起始後 12–16 週、之後每年篩檢;必要時提早。
HIV 個案|People With HIV
- HIV 增加 prediabetes/糖尿病風險。
- 部分 ARV 進一步升風險。
- A1C 在 HIV 個案可能低估糖期 → 以血糖標準診斷為佳。
- PI(protease inhibitors)與 NRTIs 風險:
- HIV 加 PI:> 5% 新發糖尿病、> 15% 為 prediabetes。
- PI 引起 insulin 阻抗,可能誘發 β 細胞凋亡。
- NRTIs 影響脂肪分布(lipohypertrophy/lipoatrophy),與阻抗相關。
- ARV 相關高血糖個案可考慮停用問題藥物(須先評估病毒控制與替代藥之副作用)。
- 仍可能需 glucose-lowering 藥物。
篩檢間隔|Testing Interval
- 最佳間隔未定。
- 3 年間隔的依據:減少需確認檢驗的偽陽,亦在偽陰者出現實質併發症前複檢。
- 高風險(接近截點、藥物使用中)者可縮短間隔。
社區篩檢|Community Screening
- 理想於健康照護場域進行(含具備資源的藥局),因需後續追蹤與治療。
- 一般不建議於非醫療場域進行(追蹤與接續照護可能不到位)。
- 若已建立轉介系統可考慮。
- 社區篩檢易瞄準錯人(漏掉高風險、誤檢低風險或已確診者)。
牙科篩檢|Screening in Dental Practices
- 牙周病與糖尿病雙向關係 → 探索牙科場域篩檢與轉介初級照護。
- 一研究估計 ≥ 30 歲一般牙科病人 30% 為新確診血糖異常。
- 仍需更多研究驗證可行性、效益與成本效益。
兒童/青少年 prediabetes/T2D 篩檢|Screening and Testing for Prediabetes and Type 2 Diabetes in Children and Adolescents
- 用於診斷成人之 A1C/血糖標準雖建立於成人族群,但 ADA 認可於兒童/青少年使用 A1C、FPG、2-h PG。
- 兒童/青少年 T2D 過去十年明顯上升,特定高風險族裔尤甚。
- Table 2.6 為兒童基於風險之篩檢建議;Table 2.1、2.2 之截點同樣適用兒童。
DIABETES INDUCED BY SYSTEMIC ANTI-CANCER THERAPY|全身抗癌治療誘發糖尿病
Recommendations|建議事項
- 2.19 以 ICI(anti-PD-1 或 anti-PD-L1,例如 nivolumab、pembrolizumab、avelumab)、PI3Kα 抑制劑(例如 alpelisib、inavolisib)、mTOR 抑制劑(例如 everolimus)開始抗癌治療之個案,須衛教高血糖/高血糖危症之風險、症狀與徵象。Grade E
- 2.20 ICI 治療者,於起始前、每次回診時、若治療中或停藥後出現高血糖症狀/徵象時,測 FPG 或 random plasma glucose。Grade E
- 2.21 PI3Kα 抑制劑治療者,起始前測 FPG 或 random PG + A1C;治療前 2 週每週測 random PG,之後每 4 週測一次。Grade C;考慮治療中每 3 個月測 A1C。Grade E
- 2.22 mTOR 抑制劑治療者,起始前測 FPG 或 random PG,治療期每次回診測。Grade C;考慮每 3 個月測 A1C。
抗癌藥相關高血糖總論
- 急性與慢性內分泌異常為抗癌治療不良事件之大宗。
- 高血糖發生率 15–50%(化學治療藥物如 busulfan 或常合併之 glucocorticoid 治療)。
- 為抗腫瘤治療不良結局之風險因子。
- 受 chemotherapy、glucocorticoids、immunotherapy、PI3K/Akt/mTOR 路徑抑制劑治療者皆應接受症狀衛教與血糖監測工具。
ICI 相關自體免疫糖尿病
- PD-1(nivolumab)、PD-L1(durvalumab)抑制劑為主,anti-CTLA-4(ipilimumab)較少。
- 發生率 0.6–1.4%;常以 DKA 表現、幾乎一律需終身 insulin。
- 起病高峰於起始後 2–3 個月,但治療任何階段乃至停藥後皆可能。
- 處置:
- 比照新診 T1D 立即轉介內分泌、提供糖尿病自我管理衛教。
- 起始前與每次回診(或症狀出現時)測 FPG 或 random PG。
- 風險預測:HLA 風險評分需更多流行病學驗證。
PI3Kα 抑制劑
- alpelisib、inavolisib 已核可於 advanced 或 metastatic 乳癌。
- 主要試驗:加入標準療法可提供存活益處,但 grade 3/4 高血糖達 36% 為最常見停藥原因。
- 一 phase 3 RCT 後分析:alpelisib 誘發高血糖的中位起始時間 13 天,範圍可達約 1 年。
- 監測:
- 起始前測 FPG 與 random PG。
- 治療前 2 週每週測 random PG;之後每 4 週或症狀時提早。
- 可考慮每 3 個月測 A1C,但 A1C 單獨可能無法捕捉早期高峰。
mTOR 抑制劑
- everolimus 等高血糖嚴重度多變、無確切起病高峰。
- 大型 meta-analysis(3,900 人,9 RCTs,everolimus):
- All-grade 高血糖 27%
- Grade 3 與 4 為 2.5%
- 單中心回顧:cancer + everolimus 個案高血糖發生中位 5–6 個月,分布從數週至數年。
- 監測:
- 起始前 + 每次回診測 FPG 或 random PG,症狀時提早。
- 可考慮每 3 個月測 A1C。
其他
- Akt 抑制劑(capivasertib)、antibody drug conjugates(enfortumab vedotin)亦可頻發高血糖;本指引未深入。
PANCREATIC DIABETES OR DIABETES IN THE CONTEXT OF DISEASE OF THE EXOCRINE PANCREAS|胰臟性糖尿病
Recommendation|建議事項
- 2.23 急性胰臟炎發作後 3–6 個月與每年篩檢糖尿病;慢性胰臟炎建議每年篩檢。Grade E
概念與病因
- 胰臟性糖尿病(亦稱 pancreatogenic diabetes、type 3c diabetes)涵蓋:
- 結構(正常胰臟組織破壞或切除)
- 功能(外分泌胰臟功能不全 + insulin 分泌喪失)
- 常被誤診為 T2D。
- 病因多元:
- 急性/慢性胰臟炎(含發炎、纖維化導致內、外分泌功能流失)
- 創傷或胰臟切除
- 新生贅瘤
- Cystic fibrosis(後段詳述)
- Hemochromatosis
- Fibrocalculous pancreatopathy
- 罕見遺傳性疾病
- 原發型
- 「Pancreatic diabetes」為較佳統稱用語。
急性/慢性胰臟炎
- 單次急性與慢性胰臟炎皆可導致 postpancreatitis diabetes mellitus。
- 鑑別線索:
- 同時 exocrine pancreatic insufficiency(建議測 fecal elastase)
- 胰臟影像異常(endoscopic ultrasound、MRI、CT)
- 無 T1D 自體抗體
- 微血管併發症風險與其他型相當。
治療考量
- 增加胰臟炎風險之 glucose-lowering 藥物(incretin-based)應避免。
- 早期啟用 insulin。
- 胰臟切除情境:
- 反覆難治慢性胰臟炎可在專業中心考慮 islet autotransplantation 以保留內生 islet 功能。
Cystic Fibrosis–Related Diabetes|CFRD
Recommendations|建議事項
- 2.24a 所有 CF 個案於 ≥ 10 歲開始每年 CFRD 篩檢,首選 OGTT。Grade B
- 2.24b OGTT 不可行時可採 A1C 兩步策略:A1C 5.5–6.4%(37–47 mmol/mol)者於 3 個月內進行 OGTT。Grade C;A1C ≥ 6.5%(≥ 48 mmol/mol)符合 CFRD 診斷。Grade B
- 2.25 CFRD 確診後 5 年起每年並行併發症監測。Grade E
流行病學與機轉
- CFTR 蛋白基因隱性突變導致的多系統 autosomal recessive 疾病。
- CFRD 為 CF 常見共病,與 T1D/T2D 不同,常合併 exocrine pancreatic insufficiency。
- 盛行率:青少年約 20%、成人約 50%。
- 與較差營養狀態、增加 morbidity 與 mortality 相關。
- 主要缺陷為 insulin 分泌不足;伴隨疾病或 glucocorticoid 治療下亦可有阻抗。
篩檢策略
- 10 歲開始每年篩檢;OGTT 為首選(具高預測值)。
- 10 歲以下篩檢可識別 IGT 進展風險,但對體重、身高、BMI、肺功能無已建立之益處。
- 現實:僅 30–40% 成人 CF 個案每年完成 OGTT。
- A1C 兩步策略:
- 256 名 10–18 歲 CF 個案研究:A1C 5.5% 與 5.8% 對 OGTT 確診 CFRD 的敏感度分別為 91% 與 95%。
- A1C 5.5% 對 CFRD 之陰性預測值約 98% → 適合作為第一線篩檢工具。
- 僅 A1C 5.5–6.4% 者進入 OGTT。
- A1C ≥ 6.5%(≥ 48 mmol/mol)即符合 CFRD 診斷,宜以 A1C 重複或 OGTT 確認(FPG 在 CF 敏感度較低)。
- 體重下降或預期增重失敗為篩檢觸發。
- Cystic Fibrosis Foundation Patient Registry(3,553 人,13% CFRD):早期診斷與治療可保存肺功能。
- CGM 可較 OGTT 更早捕捉 dysglycemia,但缺驗證閾值,目前不建議於研究外使用。
- 高效 CFTR 調節劑治療下是否調整篩檢,現有證據不足。
治療
- 臨床試驗資料有限。
- 應以 insulin 達個別化血糖目標。
POSTTRANSPLANTATION DIABETES MELLITUS|PTDM
Recommendations|建議事項
- 2.26 器官移植後篩檢高血糖;正式 PTDM 診斷宜於免疫抑制方案穩定、無急性感染時做出。Grade B
- 2.27 OGTT 為 PTDM 診斷首選。Grade B
- 2.28 免疫抑制方案應選擇對個案與移植存活最佳者,與 PTDM 風險無關。Grade E
名詞釐清
- New-onset diabetes after transplantation(NODAT):移植後新發糖尿病;排除孕前未診糖尿病與出院前已緩解之高血糖。
- Posttransplantation diabetes mellitus(PTDM):移植後出現糖尿病,不論發生時序。
- 臨床意義:PTDM 為 solid-organ 移植中 CV 與 CKD 之顯著風險因子。
早期高血糖
- 90% 腎移植受者於移植後數週內高血糖。
- 多數於出院前緩解(壓力或 glucocorticoid 引發)。
- 雖然免疫抑制治療為 PTDM 主要貢獻者,但移植排斥風險高於 PTDM;糖尿病照護角色為適當治療高血糖,不論免疫抑制種類。
風險因子
- 一般糖尿病風險:年齡、家族史、肥胖。
- 移植特異:免疫抑制劑類別與組合。
診斷時機與工具
- 早期高血糖為後續 PTDM 之風險因子。
- 正式 PTDM 診斷宜於 maintenance 免疫抑制穩定(通常 3 個月)、無急性感染時建立。
- OGTT 為診斷工具(最早可於移植後 3 個月)。
- FPG 與 A1C 可作篩檢以辨識需 OGTT 評估之高風險者,並減少 OGTT 總量。
治療
- glucose-lowering 藥物之短/長期 RCTs 數量少。
- 多數研究:移植後高血糖/PTDM 者排斥率、感染、再住院較高。
- 院內:insulin 為首選,可延續至出院後。
- 長期:noninsulin 藥物可考慮;選擇基於副作用、免疫抑制交互作用、CV 與 kidney 益處。
MONOGENIC DIABETES SYNDROMES|單基因型糖尿病
Recommendations|建議事項
- 2.29a 不論目前年齡,所有出生 6 個月內被診斷糖尿病者應接受 neonatal diabetes 基因檢測。Grade A
- 2.29b 兒童與年輕成人若不具典型 T1D/T2D 特徵且具家族多代糖尿病史(提示 autosomal dominant 模式)者應接受 MODY 基因檢測。Grade A
- 2.29c 兩種情境皆建議轉介專精糖尿病遺傳之中心,了解突變意涵與後續評估、治療與遺傳諮詢方法。Grade E
概論
- β 細胞功能異常(如 neonatal diabetes、MODY)或 insulin 阻抗症候群(如 monogenic lipodystrophy)所致之單基因缺陷,占糖尿病 < 5%。
- Table 2.7 列舉最常見原因。
- 全面清單見 Genetic Diagnosis of Endocrine Disorders 與 ISPAD 2022 共識指引。
診斷觸發
- 應考慮單基因型糖尿病之臨床線索:
- 出生後 6 個月內診斷糖尿病
- 不具典型 T1D/T2D 特徵:糖尿病自體抗體陰性、無肥胖、缺乏其他代謝特徵、強烈家族史
- 穩定、輕度禁食高血糖(FPG 100–150 mg/dL[5.6–8.5 mmol/L])、A1C 5.6–7.6%(38–60 mmol/mol),尤其無肥胖
Neonatal Diabetes|新生兒糖尿病
- 6 個月以下發病者稱為 neonatal diabetes,80–85% 可找到單基因型病因。
- 6 個月以上發病罕見;自體免疫 T1D 在 6 個月以下罕見。
- Neonatal diabetes 可暫時或永久:
- Transient:多數源於 6q24 chromosome 上基因過度表現;約半數復發;可能可用 insulin 以外藥物治療。
- Permanent:最常見為 KCNJ11(Kir6.2)與 ABCC8(SUR1)之 autosomal dominant 突變(β 細胞 K_ATP channel)。
- ADA-EASD T1D 共識報告建議:不論目前年齡,6 個月以下發病者應行基因檢測。
- 治療意涵:
- 30–50% K_ATP-related 個案改用高劑量 oral sulfonylurea 取代 insulin 後血糖改善。
- INS 突變(neonatal diabetes 第二常見原因)以 insulin 為首選。
Maturity-Onset Diabetes of the Young|MODY
- 常以年輕(典型 < 25 歲,亦可較晚)發病高血糖為特徵。
- Insulin 分泌受損,insulin 作用通常無或僅微缺陷(無共病肥胖)。
- 為 autosomal dominant;目前已找出 14 個以上基因,分布於不同 chromosome。
- 最常見:
- GCK-MODY(MODY2)
- HNF1A-MODY(MODY3)
- HNF4A-MODY(MODY1)
- 正確診斷重要原因:
- 誤診為 T1D/T2D → 治療次佳甚至有害
- 影響家屬診斷
- 評估:
- 非典型糖尿病 + 多家庭成員具非典型糖尿病 → 考慮 MODY。
- T1D 自體抗體存在通常排除單基因型(少數仍可共存)。
- 疑似者應行基因檢測(next-generation sequencing 漸普及且具成本效益)。
- 推薦轉介專精糖尿病遺傳中心。
- 遺傳諮詢以協助個案了解遺傳模式與診斷重要性。
- 治療差異:
- GCK-MODY:通常無需治療
- HNF1A-MODY、HNF4A-MODY:sulfonylurea 為一線治療
- 額外辨識家屬與胰臟外併發症之機會。
Table 2.7:最常見單基因型糖尿病原因|Most Common Causes of Monogenic Diabetes
| 類別 | 基因 | 遺傳 | 臨床特徵 |
|---|---|---|---|
| MODY | HNF1A | AD | HNF1A-MODY:青少年至成人早期發病的進行性 insulin 分泌缺陷;腎糖閾下降;OGTT 2-h PG 大幅上升(> 90 mg/dL[> 5 mmol/L]);hs-CRP 偏低;對 sulfonylurea 敏感。 |
| MODY | GCK | AD | GCK-MODY:葡萄糖刺激 insulin 分泌之閾值(set point)較高,造成穩定、不進行性的禁食高血糖;非妊娠者通常無需治療;微血管併發症罕見;OGTT 2-h PG 上升較小(< 54 mg/dL[< 3 mmol/L])。 |
| MODY | HNF4A | AD | HNF4A-MODY:青少年至成人早期發病的進行性 insulin 分泌缺陷;可能 macrosomia 與 transient neonatal hypoglycemia;對 sulfonylurea 敏感。 |
| MODY | HNF1B | AD | HNF1B-MODY:發育性腎臟疾病(多為 cystic)、泌尿生殖異常、胰臟萎縮、hyperuricemia、gout。 |
| Neonatal(permanent) | KCNJ11 | AD | IUGR;可能發育遲緩與抽搐;對 sulfonylurea 反應佳。 |
| Neonatal(permanent) | ABCC8 | AD | IUGR;少數發育遲緩;對 sulfonylurea 反應佳。 |
| Neonatal(permanent) | INS | AD | IUGR;需 insulin。 |
| Neonatal(permanent) | FOXP3 | X-linked | IPEX syndrome:自體免疫糖尿病、自體免疫甲狀腺疾病、剝脫性皮膚炎;需 insulin。 |
| Neonatal(transient) | 6q24(PLAGL1、HYMA1) | AD(父系重複) | IUGR;macroglossia;umbilical hernia;可能可用 insulin 以外藥物治療。 |
[!tip]- Table 2.7 讀表教學
- MODY 部份依基因辨識治療策略:GCK 通常觀察、HNF1A/HNF4A 偏 sulfonylurea。
- HNF1B 對應 renal cysts and diabetes syndrome(RCAD),須評估腎臟與泌尿生殖系統。
- K_ATP 通道(KCNJ11/ABCC8)為 sulfonylurea 反應特別佳之 neonatal diabetes 原因。
- 6q24 涉及 imprinting 與父系 duplication;多為暫時性。
- 縮寫:AD=autosomal dominant;AR=autosomal recessive;IUGR=intrauterine growth restriction;UPD6=uniparental disomy of chromosome 6;2-h PG=2-h plasma glucose;OGTT=oral glucose tolerance test。
GESTATIONAL DIABETES MELLITUS|妊娠糖尿病
Recommendations|建議事項
- 2.30 計畫懷孕者,具風險因子者(Table 2.5)篩檢未診 prediabetes/糖尿病;Grade B;可考慮對所有計畫懷孕者進行篩檢。Grade E
- 2.31a 妊娠 < 15 週,具風險因子者(Table 2.5)首次產檢以非妊娠標準篩檢未診糖尿病;Grade B;可考慮對所有人篩檢。Grade E
- 2.31b 妊娠 < 15 週,篩檢 abnormal glucose metabolism(A1C 5.9–6.4%[41–47 mmol/mol]或 FPG 110–125 mg/dL[6.1–6.9 mmol/L])以識別後續妊娠/新生兒不良結果與後期 GDM 高風險者。Grade B
- 2.32 24–28 週篩檢 GDM(先前未診糖尿病或本次妊娠早期高風險異常者)。Grade A
- 2.33 GDM 個案於產後 4–12 週以 75-g OGTT 與非妊娠診斷標準篩檢 prediabetes/糖尿病。Grade B
- 2.34 GDM 史者終身每 1–3 年篩檢 prediabetes/糖尿病發展。Grade B
Definition|定義
- 過去:妊娠中首次認知之任何程度葡萄糖耐受異常皆為 GDM(不論高糖程度)。
- 此舊定義之限制:
- 多數 GDM 案例其實為孕前已存在之高血糖,因孕前未常規篩檢而於孕期被識別。
- 肥胖/糖尿病流行 → 育齡期 T2D 增加 → 早期妊娠中未診 T2D 個案增加。
- 理想:孕前診斷未知糖尿病,特別是具風險因子或高風險族群者,可由 preconception care 受益。
- 已知糖尿病之 preconception care:A1C 較低、出生缺陷、preterm delivery、perinatal mortality、SGA、NICU 入院率較低。
- 若孕前未篩,妊娠 < 15 週可考慮普篩(非選擇性)以辨識未診糖尿病,特別是高盛行率族群。
- 種族/族群差異存在於未診糖尿病盛行率 → 早期篩檢為解決健康不平等之第一步。
- 早期妊娠未診糖尿病之診斷標準同非妊娠者(Table 2.1)。
- 若診出糖尿病應分類為「複合妊娠之糖尿病」(多為 T2D,少數 T1D 或單基因型)並依此處置。
- Early abnormal glucose metabolism 範圍:
- FPG ≥ 110 mg/dL(6.1 mmol/L)
- A1C ≥ 5.9%(41 mmol/mol)
- 與妊娠/新生兒不良結局(preeclampsia、macrosomia、shoulder dystocia、perinatal death)相關,且與後續 GDM 高風險相關。
- 部分研究顯示 A1C ≥ 5.7% 即與不良 perinatal 結局相關。
- 各專業學會早孕期低於顯性糖尿病的高血糖診斷與處理建議不一致。
- 早期篩檢若為陰性,於 24–28 週重新篩 GDM;先前未篩者於 24–28 週同時間點篩。
- IADPSG 之 75-g OGTT 標準與 two-step 之 GDM 標準均未從妊娠前半段資料推導,不應用於早期篩檢。
- A1C 與 FPG 同樣為低成本檢驗:
- A1C 優點:可加入產檢實驗室、不需早晨禁食。
- 缺點:紅血球更新異常(多為下降使 A1C 偏低、上升使 A1C 偏高)、hemoglobinopathies、缺鐵性貧血(升 A1C)。
- GDM 常為內在 β 細胞功能異常之指標 → 母體日後葡萄糖不耐受/糖尿病風險顯著上升。
- GDM 個案應終身篩檢 prediabetes/T2D,以便早期介入與治療。
Diagnosis|診斷
- HAPO study(> 23,000 名孕婦):母體 24–28 週血糖與多項母/胎/新生兒不良結局呈連續性增加;多數併發症無風險閾值。此結果引發 GDM 診斷標準重新審視。
- 兩種診斷策略(Table 2.8):
- One-step:依 IADPSG 衍生之 75-g OGTT。
- Two-step:較早期之 50-g 非禁食篩檢 → 螢幕陽性者進 100-g OGTT,依 Carpenter-Coustan 對 O’Sullivan-Mahan 之解讀。
Table 2.8:GDM 篩檢與診斷|Screening for and Diagnosis of GDM
One-step strategy|一步策略
- 24–28 週對未診糖尿病者進行 75-g OGTT。
- 抽血時點:禁食、1 h、2 h。
- OGTT 應於早晨、≥ 8 h 過夜禁食後進行。
- 任一以下血漿葡萄糖達標即診斷 GDM:
- 禁食:92 mg/dL(5.1 mmol/L)
- 1 h:180 mg/dL(10.0 mmol/L)
- 2 h:153 mg/dL(8.5 mmol/L)
Two-step strategy|兩步策略
- Step 1
- 24–28 週對未診糖尿病者進行 50-g GLT(非禁食),1 h 測血漿葡萄糖。
- 1 h 結果 ≥ 130、135 或 140 mg/dL(7.2、7.5 或 7.8 mmol/L)(ACOG 認可任一)→ 進入 100-g OGTT。
- Step 2
- 100-g OGTT 須禁食。
- Carpenter-Coustan 標準:禁食、1、2、3 h 中,至少兩個達/超達標即診斷 GDM。
- 截點:
- 禁食:95 mg/dL(5.3 mmol/L)
- 1 h:180 mg/dL(10.0 mmol/L)
- 2 h:155 mg/dL(8.6 mmol/L)
- 3 h:140 mg/dL(7.8 mmol/L)
- ACOG 註:單一達標亦可作為診斷依據。
[!tip]- Table 2.8 讀表教學
- One-step:「75-g OGTT,三點任一達標即診斷」,截點較低、診斷數量較高。
- Two-step:「50-g GLT 篩 → 100-g OGTT 確認」,篩檢無需禁食、確診需兩值達標(ACOG 允許一值)。
- One-step 截點來自妊娠終點(HAPO odds 1.75);two-step 截點為更早期 maternal-outcome 衍生。
- 不同截點 → 不同高血糖嚴重度與母/胎風險識別 → 解釋專家學會推薦差異。
One-Step Strategy|一步策略
- IADPSG 自 HAPO 衍生:以 24–28 週孕婦中 odds 達不良結局 1.75 倍處之 OGTT 平均 fasting、1 h、2 h 葡萄糖為截點。
- 預期將使 GDM 發生率由 5–6% 增至 15–20%(主因僅需一個異常值即可診斷)。
- 區域研究:使用 IADPSG 標準後 GDM 案例增 1–3 倍。
- 後續資料:
- 11 年盲性 follow-up 顯示,依 one-step 標準將被診為 GDM 者,相較未 GDM,發展為 prediabetes/T2D 風險高 3.4 倍,後代肥胖與體脂風險增加 → 此族群可由產後加強篩檢受益。
- ADA 推薦 IADPSG 標準以最佳化妊娠結局,因其唯一以妊娠結局為依據(其他標準以母體後期糖尿病等終點推導)。
- 介入研究(針對較舊標準下相對輕度 GDM)顯示介入帶來中等效益:減少 LGA 與 preeclampsia 發生率。
- 80–90% 輕度 GDM 可僅以 lifestyle 治療管理。
- OGTT 截點與 IADPSG 重疊;某試驗 2-h PG 截點 140 mg/dL 低於 IADPSG 153 mg/dL。
- 沒有 RCTs 比較不同標準下「治療 vs 不治療」GDM。
- 一隨機試驗(24–28 週以 one-step IADPSG 與 two-step Carpenter-Coustan 對比):
- One-step 識別出兩倍 GDM 個案。
- 治療人數較多但兩組妊娠/周產期併發症無差異。
- 試驗存在樣本估計與 protocol 順從度疑慮(two-step 組 165 名未列為 GDM 者因孤立 FPG > 95 mg/dL 接受治療)。
- 長期意義:
- One-step 識別 maternal long-term prediabetes/diabetes 風險與 offspring 葡萄糖不耐受/脂肪堆積之風險。
- HAPO cohort 後設分析:one-step GDM 個案後代於 10–14 歲時 IGT 較高、OGTT 多時點 glucose 較高、insulin sensitivity 與 oral disposition index 下降;母體 fasting/1-h/2-h 與後代代謝結果連續關聯。
- HAPO Follow-up Study:新生兒體脂與胎兒高 insulin 血症(cord C-peptide)為兒童體脂之中介因子。
- 目前不足之處:缺乏母親妊娠期高血糖治療對後代肥胖/糖尿病/代謝疾病之影響資料;需更多設計良好之試驗。
Two-Step Strategy|兩步策略
- 2013 NIH 共識會議:建議延續 two-step 策略(1-h 50-g GLT → 篩檢陽性者進 3-h 100-g OGTT)。
- ACOG 建議 1-h 50-g GLT 以 130/135/140 mg/dL 任一為截點。
- 2021 USPSTF 系統回顧:one-step vs two-step 對 GDM 發生率(11.5% vs 4.9%)有差,但無健康結局改善。
- 妊娠 24–28 週 A1C 篩檢 GDM 表現不如 GLT。
- NIH panel 提醒:缺乏 one-step 益處之臨床試驗證據;one-step 大量診斷可能帶來醫療化、健康照護利用與成本上升。
- 50-g GLT 不需禁食、操作較容易。
- 治療較高閾值之高血糖(two-step 識別):
- 減少 macrosomia、LGA、shoulder dystocia
- 不增加 SGA
- ACOG 目前支持 two-step,但提醒可採單一達標而非雙達標進行 GDM 診斷(若採此策略,GDM 發生率將顯著增加)。
- 3-h 100-g OGTT 兩套截點(皆為 O’Sullivan-Mahan 原始閾值之數學換算):
- Carpenter-Coustan(較低)
- National Diabetes Data Group(較高)
- 一輕度 GDM 識別/治療 RCT 之次級分析:治療在符合 Carpenter-Coustan 較低截點與符合 NDDG 較高截點兩組皆相似獲益。
- 若採 two-step,推薦 Carpenter-Coustan 較低截點。
Future Considerations|未來方向
- 兩種策略各有支持資料。
- GDM 篩檢之經濟評估系統回顧:one-step 識別更多 GDM、較可能具成本效益。
- 策略選擇取決於:
- 是否願意依 correlation studies(而非介入試驗)改變實務
- 既有基礎建設
- 成本考量
- IADPSG(one-step)已成為國際偏好之策略。
- 比較人口層級 one-step vs two-step 結果之資料目前仍不一致。
- 依 IADPSG 標準應診而未識別之 GDM 妊娠,其結果與 two-step 嚴格標準下確診者相似。
- 共識:建立統一 GDM 診斷將有利病人、照護者與政策制定者。
- 長期結局研究持續進行。
—— 本章結束 ——
TEACHING SLIDES
ADA 2026 §2|糖尿病的診斷與分類
01 診斷四選一
- A1C ≥ 6.5%(NGSP/DCCT)
- FPG ≥ 126 mg/dL(禁食 ≥ 8 h)
- 75-g OGTT 2-h PG ≥ 200 mg/dL
- 症狀/危症 + random PG ≥ 200 mg/dL
02 確診規則
- 無不模糊高血糖時須兩次異常
- 同次抽血兩項不同檢驗即可
- 或同檢驗兩個時間點
- 不一致時複測達截點之檢驗
03 糖尿病前期
- A1C 5.7–6.4%(39–47 mmol/mol)
- IFG:FPG 100–125 mg/dL
- IGT:2-h PG 140–199 mg/dL
- T2D 預防證據主要來自 IGT ± IFG
04 三檢查比較
- FPG/A1C:易行、低變異
- 2-h PG:敏感度最高
- A1C 免禁食、穩定
- 圖:Table 2.3
05 A1C 限制
- Hemoglobin variants(如 sickle cell trait)
- G6PD G202A:黑人男性同合子降 0.8%
- 貧血、CKD/透析、HIV、erythropoietin
- 妊娠 → 改用血糖標準
06 OGTT 注意
- 前 3 日 ≥ 150 g/day 碳水
- 限制碳水 → 偽陽
- CFRD、PTDM 偏好 OGTT
- 非禁食 50-g GLT 用於 GDM two-step
07 分類四類
- T1D:自體免疫 β 細胞破壞(含 LADA)
- T2D:β 細胞分泌缺陷 + 胰島素阻抗
- 其他特異型:單基因、外分泌胰臟、藥物
- GDM:妊娠中後期新發
08 AABBCC 鑑別
- Age(< 35 y)
- Autoimmunity
- Body habitus(BMI < 25)
- Background(家族史)
- Control(noninsulin 無法達標)
- Comorbidities(如 ICI)
09 T1D 三階段
- Stage 1:多抗體 + 正常血糖
- Stage 2:抗體 + dysglycemia
- Stage 3:顯性高血糖
- 圖:Table 2.4
10 T1D 風險
- Stage 1 5 年發病 ~44%
- Stage 2 → 3:2 年 ~60%、5 年 ~75%
- 多抗體者 10–15 年進展 70–84%
- 兒童 25–50% 起病以 DKA
11 T1D 抗體
- GAD(首選)
- IA-2、ZnT8、IAA
- 單一 IA-2 同多抗體風險
- 多抗體可考慮 teplizumab
12 T1D 監測頻率
- ≤ 3 歲:6 mo × 3 y → 1 y × 3 y
- 3–18 歲:每年;3 年無進展可停
- 成人:每 3 年(高風險每年)
- 抗體 + random glucose + A1C
13 ICI 誘發糖尿病
- 0.6–1.4% 發生率
- 常以 DKA 表現、需終身 insulin
- 多在治療後 2–3 個月發病
- 起始前、每次回診測 PG
14 PI3Kα/mTOR 抑制劑
- alpelisib:grade 3–4 高血糖 36%
- 中位起始 13 天
- everolimus:all-grade 27%
- 中位起始 5–6 個月
15 T2D 篩檢入口
- 35 歲全民起篩
- 任何年齡 BMI ≥ 25(亞裔 ≥ 23)+ 風險
- 陰性 ≥ 3 年複檢
- 圖:Table 2.5
16 兒童 T2D 篩檢
- 青春期或 ≥ 10 歲(早者)
- BMI ≥ 85 / 95 百分位
- + 一個以上風險因子
- 圖:Table 2.6
17 藥物相關糖尿病
- Glucocorticoids:餐後/random PG 監測
- 第二代抗精神病:起始、12–16 週、每年
- HIV/ARV:FPG 起始、轉換、3–6 mo
- Statins、thiazide、HIV PI 增風險
18 胰臟性糖尿病
- 急性/慢性胰臟炎、切除、CF
- Hemochromatosis、neoplasia
- 鑑別:fecal elastase 低 + 影像 + 抗體陰性
- 避免 incretin 類藥物
19 CFRD
- ≥ 10 歲每年篩
- OGTT 為首選
- A1C 5.5–6.4 → OGTT;≥ 6.5 直接診斷
- 治療 = insulin
20 PTDM
- 早期 90% kidney 受者高血糖
- 多於出院前緩解
- 正式診斷宜 ≥ 3 個月免疫抑制穩定
- OGTT 為首選
21 單基因型概論
- 占 < 5%
- 6 個月內發病:必檢測
- T1D/T2D 非典型 + 多代家族史
- 圖:Table 2.7
22 Neonatal diabetes
- 6 mo 內發病 80–85% 為單基因
- KCNJ11/ABCC8 → 高劑量 sulfonylurea
- 30–50% 改用後血糖改善
- INS 突變 → insulin
23 MODY
- AD、14+ 基因
- GCK:通常觀察
- HNF1A/HNF4A:sulfonylurea 一線
- HNF1B:腎囊腫 + 痛風
24 GDM 時間軸
- 計畫懷孕:風險因子篩
- < 15 週:篩未診糖尿病、abnormal glucose(A1C 5.9–6.4 或 FPG 110–125)
- 24–28 週:one-step 或 two-step
- 產後 4–12 週:75-g OGTT 重新分類
25 One-step(IADPSG)
- 24–28 週 75-g OGTT
- FPG 92 / 1-h 180 / 2-h 153 mg/dL
- 任一達標即 GDM
- ADA 推薦(HAPO 結局推導)
26 Two-step
- 1-h 50-g GLT(非禁食)≥ 130 / 135 / 140
- 3-h 100-g OGTT(Carpenter-Coustan)
- 兩值達標(ACOG 接受一值)
- ACOG 偏好;USPSTF 二者結局相似
27 GDM 終身追蹤
- 4–12 週:75-g OGTT
- 終身每 1–3 年篩
- β 細胞功能異常指標
- 介入可預防後續 T2D