Williams Endocrinology 15e Ch34|第 2 型糖尿病的治療
KEY TAKEAWAYS
- T2D 治療在過去 20 年完成轉型:可用藥物大幅擴張,多數患者可安全降糖至接近正常範圍。診斷以 FPG ≥ 126、2-hr PG ≥ 200、HbA₁c ≥ 6.5% 或具症狀的隨機血糖 ≥ 200 為依據;HbA₁c 標準化後優於空腹/糖耐受試驗,但同一人的 HbA₁c 與葡萄糖可能存在「糖化裂隙」(glycation gap) ≥ 0.3–0.4% 需辨識。
- 介入研究結論可分三類訊息。UKPDS:sulfonylurea/insulin 強化治療使微血管事件下降 25%、20 年後 MI 下降 15%、總死亡下降 13%(legacy effect);metformin 組(過重者)的 MI 降 33%、總死亡降 27%。ACCORD/ADVANCE/VADT:高心血管風險族群中,HbA₁c < 6% 並未帶來複合心血管益處,ACCORD 強化組總死亡上升 22%;後續分析顯示死亡集中於「目標 < 6% 卻無法降到 < 7%」的個體,並非已達成低 HbA₁c 者。
- ADA 一般 HbA₁c 目標 < 7%(高風險者放寬至 7–8%;新發病、預期壽命長、無 CVD 者可更嚴格);ACE 為 ≤ 6.5%。空腹/餐前 80–130 mg/dL,餐後 < 180 mg/dL;無證據支持單獨針對餐後血糖的具體目標。
- 監測工具:HbA₁c 反映 2–3 個月平均;SMBG 對使用 insulin 或 sulfonylurea、新診斷、控制不穩、孕婦特別重要;CGM 在使用強化 insulin 治療的 T2D 已驗證有益、Medicare 已給付;CGM 可量測平均血糖、辨識「糖化裂隙」並降低低血糖風險。
- 低血糖三級分法(ADA):Level 1 < 70 且 ≥ 54 mg/dL(警示值)、Level 2 ≤ 54 mg/dL(臨床顯著、需立即處置)、Level 3 需他人協助(嚴重)。Level 3 為跌倒、心血管事件、死亡的標誌;通常與共病、營養不良、衰弱、認知功能減退並存。
- DSMES(diabetes self-management education and support)為 T2D 治療基石,可降 HbA₁c 0.45–0.57%、減少併發症、降低死亡與成本;應於診斷時、每年、出現併發症時、生活/醫療轉變時提供。實際使用率 ≤ 7%(私人保險)、5%(Medicare 第 1 年)。
- 醫療營養治療 (MNT):6 個月內 3–6 次諮詢,可降 HbA₁c 0.3–2.0%。減重 5% 帶來臨床代謝益處;體重下降 > 15% 者 86% HbA₁c < 6.5%。比起特定巨量營養素分布,總熱量降低與維持更重要;減少碳水化合物對血糖最有證據;避免含糖飲料。地中海、DASH、低碳水、植物為基礎飲食皆可採用。
- Metformin 為 T2D 的首選初始藥物(無禁忌時),HbA₁c 下降 1.0–2.0%;機轉包含活化 AMPK、抑制 mitochondrial glycerophosphate dehydrogenase、腸道作用增加 GLP1。eGFR 45–59 可用;30–44 考慮減量;< 30 禁用。最常見不良反應為胃腸道;少數人 vitamin B₁₂ 缺乏(可補充 1000 μg/d)。乳酸性酸中毒罕見且幾乎只見於本身高風險者。可不需停藥,即使 HbA₁c < 6.5%。
- Sulfonylurea:作用於 SUR1 / KATP,引起 glucose-independent 然後 glucose-dependent 的 insulin 釋放;HbA₁c 下降 0.5–1.5%。主要缺點:低血糖、體重增加、效力衰退(glyburide 最明顯)。Glyburide 對 SUR2 結合可能干擾 ischemic preconditioning,較不建議;目前以 glimepiride、ER glipizide、ER gliclazide 為首選。CAROLINA 顯示 glimepiride 與 linagliptin MACE 無差異。低劑量啟動(如 glimepiride 0.5–1 mg)即有效。
- TZD(pioglitazone, rosiglitazone):PPARγ agonist,改善胰島素阻抗、降 free fatty acid,HbA₁c 下降 0.75–1.5%;pioglitazone 改善 NASH、降低 stroke/TIA 後再次心血管事件、改善 dyslipidemia;副作用為體重增加(皮下脂肪 + ECF)、水腫、心衰竭、骨折(停經後女性遠端骨折最明顯)、可能 macular edema。膀胱癌證據不一致,但有膀胱癌史時避用 pioglitazone。應低劑量起始、衛教監測水腫。
- DPP4 inhibitor(sitagliptin, vildagliptin, saxagliptin, linagliptin, alogliptin):升高內生性 GLP1 約 2 倍,HbA₁c 下降 0.5–1.0%。體重中性、低血糖風險低、耐受性高。Saxagliptin 與 alogliptin 在 CVOT 顯示心衰住院增加;sitagliptin 無此訊號。胰臟炎史者禁用。Linagliptin 不需依 eGFR 調整。
- SGLT2 inhibitor(canagliflozin、dapagliflozin、empagliflozin、ertugliflozin):阻斷近端腎小管 SGLT2 → 葡萄糖、鈉排出,HbA₁c 下降 0.5–1.0%、降血壓、減重 2–3 kg、改善 NAFLD。不分糖尿病有無,皆顯示心衰住院與 CKD 進展明顯下降;EMPA-REG OUTCOME 全因死亡 RR 下降 32%。建議用於合併 ASCVD、HF、CKD 的 T2D。eGFR < 45 不建議啟動以降糖(但對心腎仍有保護),eGFR 低限再下修中。不良反應:泌尿道與生殖部位黴菌感染(女性 ≥ 10–15%)、脫水、euglycemic DKA、canagliflozin 截肢;dapagliflozin 在膀胱癌史者警告避用。
- α-Glucosidase inhibitor(acarbose、miglitol、voglibose):延緩腸道碳水化合物吸收,HbA₁c 下降 0.5–1.0%、餐後血糖最有效,無低血糖、可能減重;副作用以脹氣與腹瀉為主。Colesevelam(膽酸結合劑)、bromocriptine(多巴胺 agonist 早晨快速釋放劑型)為非主流選項。
- Insulin:T2D 治療的最後支柱。長效類包含 NPH、detemir、glargine U-100/U-300、degludec;icodec(每週一次)研發中。短效類包含 regular、aspart、lispro、glulisine、faster aspart (Fiasp)、ultrarapid lispro (Lyumjev);吸入型 Afrezza 起效最快但禁用於氣喘/COPD。Premixed insulin 方便但失去彈性、低血糖較多。Analog 比 human insulin 低血糖較少、但價格較高。U-500 用於極度胰島素阻抗。Pump 在 T2D 並未廣泛採用。
- GLP1 RA:分短效(exenatide、lixisenatide)與長效(liraglutide、ER exenatide、dulaglutide、semaglutide;oral semaglutide 為例外)。長效對基礎血糖更佳、副作用較少;短效對餐後血糖更明顯。HbA₁c 下降 1.0–1.8%、減重 2–10 kg;liraglutide 3.0、semaglutide 2.4 已批准用於減重。LEADER、SUSTAIN-6、REWIND 等 CVOT 顯示 MACE 下降 12–26%、albuminuria 進展下降;短效藥物未顯示心血管益處。SUSTAIN-6 看到 retinopathy 進展可能與快速降糖有關。MTC 家族史者避用。
- Tirzepatide(GIP/GLP1 dual agonist):HbA₁c 下降 2.3%(15 mg 週劑量、自基線 8.3%)、46% 降至 5.7%、體重下降 > 10% 達 57%;勝過 1 mg semaglutide。CVOT 尚未完成。Pramlintide(amylin analogue)為基礎與餐前 insulin 治療的輔助劑,餐前皮下注射,HbA₁c 下降 0.5–0.7%、需減 mealtime insulin 50% 以避免低血糖。
- 治療策略:先 metformin(除非禁忌或不耐);3–6 個月若 HbA₁c 未達標,加第二線。第二線依個人化考量選擇 SGLT2i、GLP1 RA、SU、TZD、DPP4i 或 basal insulin。已知 ASCVD/HF/CKD 者,SGLT2i 與/或 GLP1 RA 應提早使用而非等到 metformin 失效。GRADE 試驗(5047 人):metformin 加 glimepiride、glargine、sitagliptin、liraglutide 中 liraglutide 與 glargine 維持 HbA₁c < 7% 最持久,sitagliptin 最弱;嚴重低血糖以 glimepiride 較多,體重增加以 glimepiride 與 glargine 較多。
- 個別化策略:以心血管風險最低化、CKD 進展、低血糖最少化、體重控制、成本為軸。基礎 insulin 起始 10 U 或 0.1–0.2 U/kg;以 SMBG/CGM 早餐前血糖為標的滴定;若需餐前 insulin,1 餐起步、4 U 或 10% basal 劑量;GLP1 RA 取代或加在 basal insulin 之上常較無低血糖、較不增重。「過度 basal 化」(overbasalization) 為晚期 T2D 常見問題:HbA₁c < 8% 仍持續加 basal 劑量會增加夜間低血糖。
- 特殊狀況:嚴重高血糖呈現(HbA₁c > 10%、glucose > 300 mg/dL、ketosis)建議入院 IV insulin;非危急但 HbA₁c > 9% + retinopathy 者,6 個月內漸進降至 < 7%。Youth-onset T2D:β 細胞快速衰退,metformin 無法延緩;空腹 > 250 或 HbA₁c > 8.5% 加 basal insulin;liraglutide 已批准 ≥ 10 歲。Pregnancy:fasting < 95、1-hr < 140、2-hr < 120、HbA₁c < 6.0%;以 insulin 為主,metformin/glyburide 安全性有疑慮。
- T2D 預防:生活型態介入降進展風險 30–60%(DPP),效益持續且與減重相關;metformin 預防效力較小但對 < 60 歲、BMI ≥ 35、FPG ≥ 110、HbA₁c ≥ 6.0%、過去妊娠糖尿病者效益接近生活型態介入。Acarbose、TZD、GLP1 RA、減重手術皆可降進展。CDC National DPP 為現行公衛框架。
流行病學|Epidemiology
- T2D 為全球最常見糖尿病型態,佔 ≈ 90%。Pacific Nauru 過去糖尿病罕見、後上升至 ≈ 40% 才略降;Micronesia 仍 23–35%;South Asia 預估 2000–2025 增加 150%。
- IDF 2021 全球盛行 5.36 億 → 2045 推估 7.83 億;中收入國家增幅最大。
- 2021 全球糖尿病健保支出估 9,660 億 USD → 2045 達 1.05 兆。
- 美國 NHANES:成人糖尿病盛行 9.8%(2000)→ 14.3%(2018),未診斷比例 30.7% → 23.3%。族群分布 13.6%(白人)、15.5%(西語裔)、16.7%(非西語裔亞裔)、17.4%(非西語裔黑人);38% 美國成年人為糖尿病前期。2000 年出生男性終生罹病風險 32.8%、女性 38.5%。
- 併發症與死亡:糖尿病為失明首因,至少 40% ESRD 由糖尿病造成;心臟病與中風風險 2–4×、下肢截肢 ≈ 20×、平均減壽 10 年。雖被列為美國第七死因,因死亡證明僅 35–40% 標示糖尿病故為低估。1990–2010 間美國 MI、stroke、截肢、高血糖危機死亡率下降 ≥ 50%、ESRD 約下降 30%(截肢降幅最大);近年 ESRD 似又上升、且低收入國家數據缺乏。
- 經濟:全球直接醫療支出近 8,000 億 USD(IDF);總成本估 1.31 兆 USD 將於 2030 達 2.2 兆。美國 2017 直接醫療 3,270 億 USD;糖尿病患者人均支出為非糖尿病者 2.3×。
- 兒童 T2D:以前 < 2% 兒童糖尿病為 T2D,現在新診斷兒童糖尿病 20–25% 為 T2D(10–19 歲非歐洲族裔最高)。
診斷標準|Diagnostic Criteria
- 糖尿病診斷依據是高血糖;血糖–視網膜病變的關係為閾值估算之主要 endpoint。
- 三項常用檢驗皆能預測視網膜病變(與腎病變、神經病變、CVD):
- Fasting plasma glucose (FPG)。
- 75 g 口服葡萄糖負荷後 2 小時血糖 (2-hr PG)。
- HbA₁c。
- 診斷前期分為「糖尿病前期」與「糖尿病」(Table 34.1):
- FPG:糖尿病前期 100–125 mg/dL(5.6–6.9 mmol/L);糖尿病 ≥ 126(≥ 7.0);空腹定義為 ≥ 8 小時無熱量攝取。
- 2-hr PG(75 g OGTT):糖尿病前期 140–199(7.8–11.0);糖尿病 ≥ 200(≥ 11.1)。
- 隨機血糖:合併典型症狀且 ≥ 200(≥ 11.1)即可診斷。
- HbA₁c:糖尿病前期 5.7–6.4%(39–47 mmol/mol);糖尿病 ≥ 6.5%(≥ 48);需於認證實驗室。
- HbA₁c 優勢:標準化後變異小(個體內 CV < 2%,FPG 6.4%、2-hr PG 16.7%)、不必空腹、可預測 T2D 進展;但下列情形需注意:紅血球壽命/週轉異常、血紅蛋白變異、晚期 CKD 等。
- OGTT 為研究用途;臨床多以 FPG 異常 + 症狀 + 隨機血糖 ≥ 200 或 HbA₁c 確診,並以同一或不同方法進行確認檢驗。
一般治療策略|General Approaches to Management
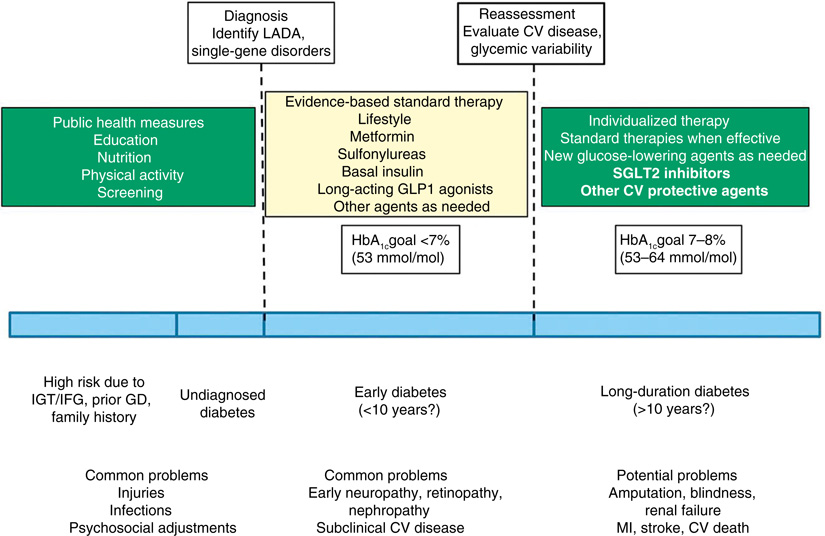
- 過去 20 年完成 T2D 群體層級的轉型:理解疾病軌跡、強調及早診斷、以系統化介入降低併發症。高血糖為微血管併發症(眼、腎、神經)以及(程度較弱)心血管事件的可改變風險因子。
- 圖 34.1(上方)以時序展示 T2D 自然史與三階段干預機會。
公共衛生措施|Public Health Measures
- 診斷前的介入:教育家庭、推動健康生活型態、限縮不健康食品行銷與分配、辨識早期高血糖(篩檢)。
一般醫療管理|Primary Care Management
- 糖尿病前期通常不需降糖藥,但其他可改變心血管風險因子需處理。
- 確診 T2D 後:併發症與高血糖嚴重度及暴露時間有關,故越早接近正常越好。初期治療多為強化生活型態 + 藥物治療;標準化簡單方案在診斷後前 10 年最有效。
複雜糖尿病照護|Complex Diabetes Care
- 病理生理進展使血糖控制日益困難;糖尿病相關與其他疾病負擔增加,限制積極治療的潛在效益。
- 約診斷 10 年後,多數需多種、常為注射型治療;個人化選擇增加;長期效益/風險不明的療法比例上升。專責團隊照護常達最佳結果。
篩檢|Screening
- T2D 盛行率仍持續上升:人口老化、易感族群成長、肥胖(久坐 + 簡單醣與高加工食品)。
- 美國診斷比例 1990 年代 ≈ 50% → 現約 77%;未診斷者於 < 中年成人尤多,CHD/stroke/PVD 風險約 2× 增加。
- Box 34.1 篩檢條件:BMI ≥ 25 kg/m²(亞洲族 ≥ 23)並具下列任一風險:一等親糖尿病、高風險族群(非洲、拉丁、原住民、亞洲、Pacific Islander)、CVD、HTN(≥ 140/90 或服藥)、HDL < 35、TG > 250、PCOS、不活動、嚴重肥胖或 acanthosis nigricans 等其他胰島素阻抗條件。糖尿病前期年檢一次;GDM 史每 ≥ 3 年;其餘 45 歲開始;正常者每 ≥ 3 年。
- 模型研究:30–45 歲開始全民篩檢、每 3–5 年一次具成本效益。HbA₁c 6.0–6.5% 者 5 年內進展糖尿病風險 25–50%(為 5% 者的 20×)。
介入研究結果|Interventional Study Results
- UKPDS:新發病 T2D 經 3 個月 diet/exercise 降 HbA₁c 由 9% → 7%;FPG > 108 後隨機分配 conventional 或 intensive;intensive 用 sulfonylurea/insulin 求 FPG < 108、metformin 部分用於 overweight 患者。
- 長期觀察 10 年 + 後續 10 年(Tables 34.2、34.3):
- sulfonylurea/insulin 組:HbA₁c 維持比 conventional 低 1%;隨年加重而上升至 8%。微血管事件 ↓ 25%(10 年)、↓ 24%(20 年);MI ↓ 16%(10 年,p = 0.052)、↓ 15%(20 年,p = 0.014);總死亡 ↓ 6%(10 年)→ 13%(20 年,p = 0.007)。低血糖需協助率 1–5%/year,最高見於 glyburide。
- metformin 組(overweight):糖尿病相關 endpoint ↓ 32% / 21%、微血管 ↓ 29% / 16%(NS)、MI ↓ 39% / 33%、總死亡 ↓ 36% / 27%。
- 體重變化在 metformin 組最少;sulfonylurea/insulin 組增加。
- 「Legacy effect」:早期良好控制持續產生效益,可能反映血管組織結構的持久變化。
- Kumamoto study(日本,正常體重 T2D):HbA₁c 9% vs 7%,6 年區間維持;微血管事件下降,CV 事件趨勢下降但未達顯著。
- 2008 年三項試驗(中老年高 CV 風險族群):
- ACCORD:HbA₁c 目標 < 6%;intensive 組總死亡 ↑ 22%。
- ADVANCE:HbA₁c ≤ 6.5%(以 gliclazide 為主);無 CV 益處。
- VADT:HbA₁c < 6%(口服 + insulin);無 CV 益處。
- 三者皆無顯著心血管複合 endpoint;多項微血管 endpoint 改善。
- ACCORD 後續分析:強化組死亡集中於「目標 < 6% 但起始較高、追蹤平均仍 > 7%」者;達 < 7% 者無增加死亡。最高三分位「HbA₁c 高於空腹葡萄糖預期」者死亡上升、無 CV 益處;中、低三分位無增死且 ≈ 25% endpoint 改善。
- 指引轉變:強調個別化目標、起始於診斷、優先採用具非降糖益處之新藥。
- meta-analysis:HbA₁c 平均下降 0.9% 對應 nonfatal MI ↓ 17%、CHD ↓ 15%;對 stroke / 全死因死亡無顯著影響。
血糖治療目標|Glycemic Treatment Targets
- ADA 一般 HbA₁c 目標 < 7%;新發病、預期壽命長、無 CVD 者可更嚴;嚴重低血糖史、預期壽命短、晚期併發症、廣泛共病或經充分治療仍 ≥ 7% 者,可放寬至 7–8% 或更高。ACE 建議 ≤ 6.5%。
- 餐前血糖目標 80–130 mg/dL(4.4–7.2 mmol/L)(ADA);ACE 建議 < 110。
- 餐後峰值(1–2 hr)目標 < 180 mg/dL(10.0 mmol/L)(ADA);ACE 為 2 hr < 140,唯多數患者疾病進展後難安全達成。
- 平均血糖 < 154 mg/dL(< 8.6 mmol/L)(依血糖剖面)。
- 高風險者:preprandial NA、PPG NA、HbA₁c 7.0–8.0%。
治療期間血糖監測|Monitoring of Glucose During Treatment
Hemoglobin A₁c
- 反映前 2–3 個月平均血糖;起始或加強治療時每 ≈ 3 個月測;穩定時 1–2 次/year。
- 限制:與「現在」血糖未必相關;個體差異(紅血球壽命/週轉、血紅蛋白變異、晚期 CKD);不評估每日變動。
- 「Glycation gap」:HbA₁c 與血糖相差 ≥ 0.3–0.4% 應辨識。
自我血糖監測|Self-Monitoring of Blood Glucose
- SMBG(毛細血糖試紙)超過 40 年;機台一般準確但日常使用變異需教育。
- 適合對象:T1D、強化 insulin 治療的 T2D、新診斷者;basal insulin 加掛口服藥的滴定需監測早餐前血糖。
- 結果並非總能改善 outcomes(單獨 SMBG 在不少 T2D 試驗未顯示獲益),但結合 self-management 可降 HbA₁c、降併發症。
- 用途:辨識症狀微弱的低血糖(即使重度低血糖在 T2D 罕見,仍可能造成跌倒、認知喪失、改變獨立生活能力);衛教、評估飲食/運動效果、激勵作用。
- 時序原則:定期變動測試時段(早晨高 vs 晚間高分布因人而異);控制不佳時先以 premeal 為主,premeal 達 120–130 後再加上 1–2 hr postprandial;新發病或 GDM 可單測餐後。
- STeP trial:每季 3 天 7 點 SMBG → 治療調整頻次與 HbA₁c 改善。
- 工具:可下載資料;患者常忘記攜帶儀器或紀錄;若診間給予重視,患者監測頻次與 HbA₁c 改善正相關。
連續血糖監測|Continuous Glucose Monitoring
- CGM 取樣皮下組織液,可實時或事後讀;T2D 採用比例日增。
- 對強化 insulin 治療的 T2D 已驗證有益。Basal insulin 滴定中的 HbA₁c 9.1% 患者使用 CGM 可改善控制與 time in range;停用後 ≈ 一半 HbA₁c 改善流失。
- 虛擬照護模式中 CGM 是核心;高使用率與滿意度(95%)。
- Medicare 已給付 T2D + insulin 患者;老年低血糖保護尤關鍵。非 insulin 治療者亦可能受益但成本效益尚未充分評估。
- CGM 提供準確平均血糖(驗證 HbA₁c 或辨識 glycation gap);圖 34.2 顯示 ambulatory glucose profile 報告。
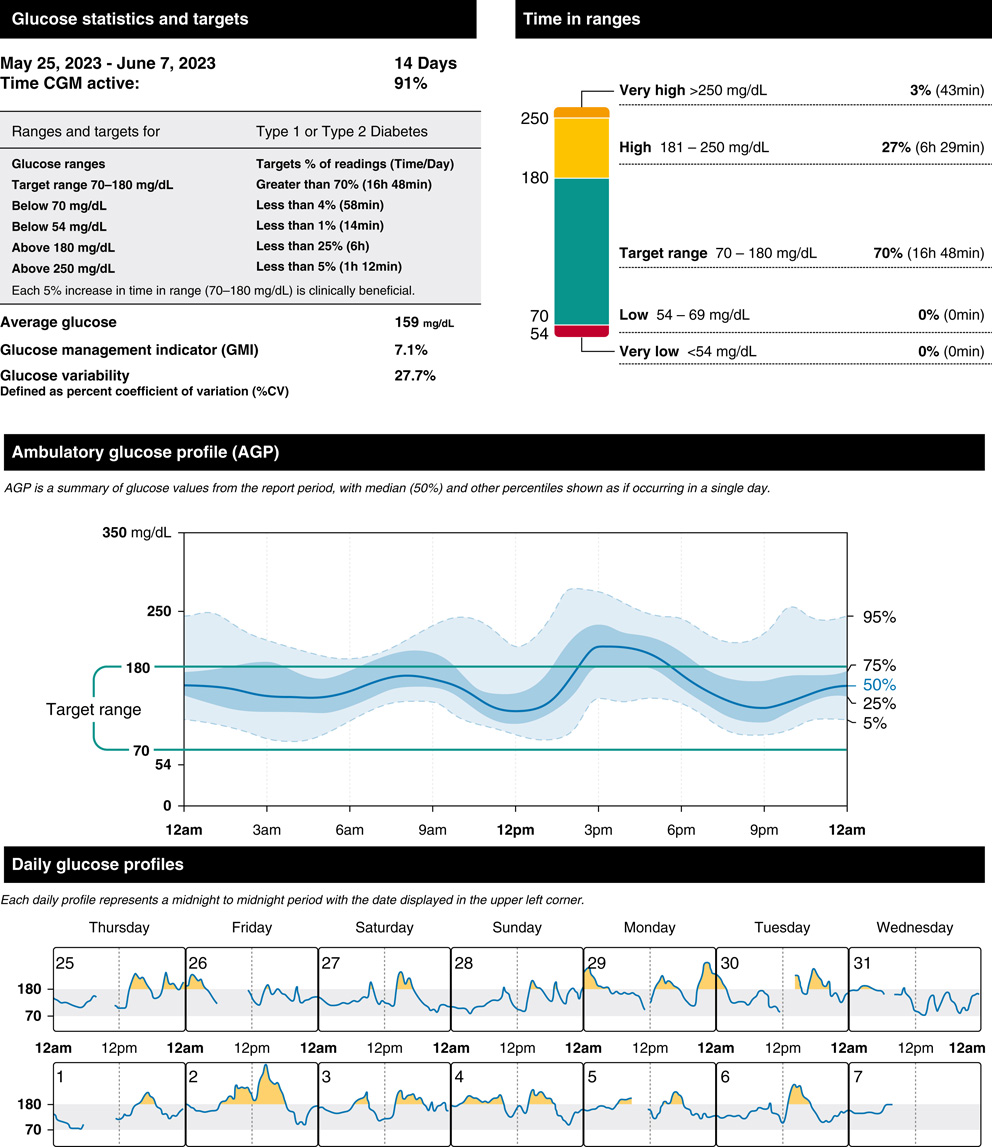
低血糖|Hypoglycemia
- ADA 三級分類(Table 34.5):
- Level 1(警示值):< 70 且 ≥ 54 mg/dL(< 3.9, ≥ 3.0 mmol/L);觸發 counterregulatory hormones(glucagon、epinephrine、norepinephrine、cortisol、GH),無症狀亦重要,需考慮調整治療。
- Level 2(臨床顯著):≤ 54 mg/dL(≤ 3.0 mmol/L);反覆出現會鈍化代償反應與警示症狀(hypoglycemia unawareness),需立即處置。
- Level 3(嚴重):心理/生理狀態改變需他人協助;與身體傷害、心血管事件、死亡強相關,部分透過跌倒/心律不整直接致害,部分反映共病、營養不良、衰弱、認知功能減退,呼籲保守化策略並重新檢視照護。
糖尿病自我管理教育與支持|Diabetes Self-Management Education and Support
- 主要生活型態介入:營養諮詢、運動建議;近年加入心理社會、壓力管理、放鬆、睡眠管理;證據強化、給付逐漸普及。
- DSMES 實證:HbA₁c ↓ 0.45–0.57%;併發症與死亡下降、QOL 改善、成本與糖尿病困擾下降。
- 應於四關鍵時點提供:診斷時、年度評估、出現併發症、生活/醫療轉變。
- 使用率低:商業保險 6.8%、Medicare 第 1 年 5%;提供者對資源缺乏認識為重要因素。
- Box 34.2 DSMES 七要件:實證治療計畫;個別化於個人需求/語言/文化、結構化課程;支持患者與家庭發展態度/信念/技能;核心內容(病理生理、用藥、監測、急慢性併發症、心理健康、特殊情況解決);於關鍵時點可得;追蹤健康狀態與 QOL;定期品質稽核。
- 團隊組成:醫師 + APP、護理、營養師、運動專家、行為治療師、藥師、足部、其他次專科。心理/認知/適應障礙常被忽略,亦影響治療結果。患者位於團隊中央,文化/信念/食物可得性/語言/經濟皆需納入。
- 非醫療人員(peer/health coach)、群體與線上社群、數位/遠距健康工具皆可貢獻。

醫療營養治療|Medical Nutrition Therapy
- MNT 為 DSMES 必要組成;理想由 RDN 提供。建議 6 個月內 3–6 次。HbA₁c 下降 0.3–2.0%。
- 在典型肥胖、年長 T2D 族群目標:減重或維持、血糖控制、足夠營養、降血壓與血脂以降 CV 風險。
- 個別化評估:每日餐次與時間、是否常漏餐、健康飲食的主要挑戰、家人是否同食、飲料種類、酒精量。
- 飲食習慣審視:果汁、即食穀片等高 GI 食物;「低碳」高脂或「低脂」高碳食物;晚餐到睡前的零食、週末過量。教導 portion control、烹調方式(油炸 vs 烤)、餐次間距、mindful eating。注意食物不安全(food insecurity)與高 HbA₁c 的關聯。
- 結構化生活型態方案可帶 5–7% 體重下降並降糖尿病風險。減重 5% 帶代謝益處比較一致;> 15% 體重下降者 86% HbA₁c < 6.5%;< 5% 者 HbA₁c 下降不顯著。
- 巨量營養素分布並無理想模式:減總熱量與維持比成份重要。碳水化合物對血糖最關鍵;T2D 多採餐前 insulin 者用 carb counting;不用 insulin 者亦需保持碳水穩定。Plate method、carb exchange、portion control 均可。
- T2D 中 β 細胞對 glucose 的立即反應消失,但第二期 insulin 分泌仍由 amino acid 與 fatty acid 驅動,故每餐含蛋白質與脂肪可緩衝 PPG。
- 低碳水/生酮飲食可降 PPG 與 HbA₁c,但部分益處可能由減重而來;長期遵守困難;空腹血糖可能反而升高。Glycemic index 在計畫中難用,研究結果不一;辨識個人飲食中高 GI 食物可能有幫助。SMBG/CGM 可確認食物對血糖之影響。
身體活動與運動|Physical Activity and Exercise
- 運動:規律有氧(每週 ≥ 150 min 中等強度,≥ 3 天,連續無 ≥ 2 天空檔)、阻力訓練 ≥ 2 次/週、避免長時間久坐。
- T2D 運動可改善 HbA₁c、insulin 阻抗、體適能、心血管風險因子;強度與量需個別化;考量併發症(PVD、retinopathy、CKD)。
- 對於 sulfonylurea/insulin 患者,運動前後監測 SMBG 並可能調整劑量;隨身碳水化合物備用。
心理社會需求|Addressing Psychosocial Needs
- 糖尿病困擾、憂鬱、焦慮、進食障礙、認知功能下降皆常見且影響治療成果。
- 建議在診斷時與後續評估,尤其在 HbA₁c 控制不佳、出現併發症、低血糖、重大生活轉變時。
- 與心理衛生、社工、行為醫學整合服務。
降糖藥物治療|Glucose-Lowering Pharmacotherapy
- 1995 後 T2D 治療因多新類別藥物加入而大幅轉型;分類已超越過去「改善敏感性 vs 增加 insulin」二分。Table 34.8 概述各類降糖藥物的給藥途徑、機轉、對 fasting/PPG/體重/BP/CV/CKD 之影響。
口服藥物|Oral Agents
- Table 34.9 總結臨床特性、劑量、禁忌、不良反應與 HbA₁c 下降程度。
雙胍類|Biguanides
- Metformin:自 1970 年代 phenformin 撤市後成為唯一可用 biguanide。
- 主要作用:抑制肝糖製造(gluconeogenesis);對周邊組織胰島素敏感性的改善較不一致;機轉仍未完全明朗。
- 活化 AMPK(細胞能量耗竭信號)、抑制 mitochondrial glycerophosphate dehydrogenase。
- 大部分作用可能透過腸黏膜接觸引發神經/激素信號至腦與其他組織;可影響 microbiome、增加 GLP1 釋放。
- 劑型:500–2000 mg/day 線性增加療效與胃腸副作用;2550 mg/day 不再增加效益;通常 BID 起始 500 mg;ER 製劑減少上消化道症狀但可能增腹瀉。HbA₁c 下降 1.0–2.0%。
- 安全性:不增加 insulin 故不致低血壙;最常見胃腸不適(≈ 1/3 早期患者);≈ 5% 即使 500 mg 也無法耐受;多伴隨體重微減或不增。
- Lactic acidosis:罕見,幾乎只見於本身高風險者。Metformin 完全由腎排除:
- 啟用前測 eGFR;eGFR < 45 不建議啟動;< 30 禁用;治療中 eGFR < 45 考慮減量、< 30 停藥。
- 肝功能不全或酗酒禁用。
- 部分患者出現 vit B₁₂ 缺乏(可能加重 PN),可補充 1000 μg/d 或定期監測。
- 證據:UKPDS 過重組 metformin → MI ↓ 39%、總死亡 ↓ 36%(10 年);20 年仍維持 33% / 27%。雖樣本較小但其他研究支持其保護效應;伴隨輕度 LDL、TG、BP 與 procoagulant 因子改善。
- 建議:所有 T2D 患者於診斷時即可啟動 metformin(無禁忌);可於糖尿病前期延緩進展,HbA₁c < 6.5% 時無須停藥。
胰島素分泌促進劑|Insulin Secretagogues
- 結合 SUR1(KATP 通道亞單位於胰島 β 細胞表面)→ 通道關閉 → 膜去極化 → L-type Ca²⁺ channel 開啟 → Ca²⁺ 上升 → insulin 分泌。
- 任何 secretagogue 第一次給藥可不依葡萄糖直接觸發 insulin 分泌;持續 SUR1 占據後此直接效應減弱,葡萄糖依賴性 potentiation 持續。
- 不同藥物的藥動、結合特性、清除路徑造成作用時間與低血糖風險不同。
磺醯基脲類|Sulfonylureas
- 早期 T2D(β 細胞功能尚保留)有效;自 1950 年代起使用;目前以 glimepiride、ER glipizide、ER gliclazide 為首選。
- 長效類藥物:單次給藥作用長,可一日一次;連續 SUR1 占據限制非依葡萄糖的 insulin 分泌但仍 potentiate 葡萄糖依賴性 basal insulin secretion;主要降空腹血糖、對 PPG 影響小、低血糖風險相對低。腎功能下降對其低血糖風險直接影響較少;chlorpropamide 例外(純腎排泄、CKD 易致嚴重低血糖,目前少用)。
- 短效類:標準 glipizide、glyburide BID 與長效效果類似但 PPG 影響大、白天進食減少時可低血糖。Glyburide 有活性代謝物腎排泄、低血糖風險最高。
- 心血管疑慮:SUR2(血管/心肌 KATP)結合可能影響 ischemic preconditioning;確認於 tolbutamide、glyburide,glimepiride/glipizide/gliclazide 較不明顯。
- 流行病學與試驗:ADVANCE(ER gliclazide)、UKPDS、CAROLINA(glimepiride vs linagliptin)皆未顯示 MACE 增加;對總死亡之影響有疑慮可能反映其他藥物之保護效應。美國使用率近 20 年下降 40%。
- 啟動建議:以 ≤ 1/4 最大劑量起始;如 glimepiride 0.5–1 mg、ER glipizide 2.5 mg;常合併 metformin 已足;高劑量增益有限。
- 缺點:低血糖、體重小幅增加、與其他藥物相比效力衰退較快(glyburide 最明顯);老人與 CKD 患者特別關注。Meta-analysis 顯示骨折較 metformin 多 25%(與 TZD 相當)。
速效胰島素分泌促進劑|Glinides
- Repaglinide:meglitinide 家族,半衰期短,與 SUR1 結合於不同位點,吸收快、在胰島素分泌的刺激較短而強;適合餐時給藥;對空腹血糖仍有些效應;劑量 0.5–4 mg/餐;高劑量增益有限。
- Nateglinide:phenylalanine 衍生物,作用更快更短;專一降 PPG,對空腹血糖影響微小;HbA₁c 下降比 repaglinide 小;適用於早期或合併其他控制空腹血糖之藥物;劑量 60–120 mg/餐。
- 對 SUR2 結合少,理論上心血管風險較低;HbA₁c 改善與 sulfonylurea 相近(repaglinide)或較弱(nateglinide);因每餐多次給藥與成本,使用有限。
噻唑啶二酮類|Thiazolidinediones
- 1997 年 troglitazone 首批,因肝毒性 2000 年退市;現可用 pioglitazone、rosiglitazone。因副作用顧慮使用偏少。
- 結合 PPAR 核轉錄因子 → 多下游效應;數週–月慢慢改善血糖、改善 insulin 阻抗、降 free fatty acid。
- Pioglitazone 對 NASH 有正效益(其餘治療有限)。Pioglitazone vs rosiglitazone:脂質效應不同——pioglitazone TG ↓ ≈ 20%、HDL 與 LDL particle size 改善;rosiglitazone TG ↑ ≈ 5%、LDL particle 數增加但 size 改善。
- 心血管:早期生理觀察支持保護(IMT、內皮功能、血脂、血壓、纖溶/凝血改善)。
- PROactive(pioglitazone 45 mg vs placebo,5238 人 T2D + 巨血管疾病):主要 endpoint 不顯著,次要 CV composite ↓ 16%(marginally);獲益被體重增加與心衰竭抵消。
- 非糖尿病、近期缺血性中風/TIA 患者,pioglitazone 降後續 stroke/MI(隨機對照)。
- RECORD(rosiglitazone 加 metformin 或 SU):CV 住院/死亡無差別;其後 meta-analysis 引發 MI 風險爭議,使 rosiglitazone 使用降低。
- ADOPT 試驗:早期 T2D,rosiglitazone 二次性血糖失敗速率比 metformin、glyburide 慢;機轉是否為 β 細胞直接效益或持續降阻抗未明。
- 不良反應:
- 體重增加(ECF 累積 + 皮下脂肪增、內臟/肝/肌內脂肪降;於 NASH 有益);應加強生活型態以限制增重。
- 水腫:使用 insulin 者與既有水腫者最易發生;衛教自我評估 pretibial edema;可加 thiazide、spironolactone、loop diuretic;嚴重水腫/HF 時停藥。PROactive、RECORD 中大劑量 TZD 增加 ≈ 2% HF 入院。
- Macular edema:報告不一。
- 骨折:藥物流行病學與試驗皆顯示停經後女性遠端骨折增加;腰椎 BMD 亦可能下降;機轉為 PPARγ 活化轉移幹細胞至 adipocyte lineage。處方前評估骨折風險與 BMD(女性尤需)。
- 膀胱癌(pioglitazone):證據不一致,整體絕對風險低;有膀胱癌史時避用。
- 起始:pioglitazone 15 mg qd,3 個月後評估;無顯著水腫且療效不足可加至 30 mg;45 mg 較難耐受。
DPP4 抑制劑|DPP4 Inhibitors
- 機轉:阻斷 DPP4 對 GLP1 之失活 → 內生 GLP1 升 ≈ 2× → glucose-dependent insulin 分泌增加、抑 basal/PPG glucagon;不影響飽足或胃排空。
- 主要降空腹血糖;HbA₁c ↓ 0.5–1.0%;體重中性、合併 metformin 不致低血糖。
- 五種藥物:sitagliptin、vildagliptin、saxagliptin、linagliptin、alogliptin;耐受性良好(adverse profile 與安慰劑近似)。
- 風險:postmarketing pancreatitis(有 pancreatitis 史者禁用);CVOT 中 saxagliptin 增加 HF 住院、alogliptin 數值不對稱;sitagliptin 無此訊號;嚴重過敏報告罕見。
- 劑量:linagliptin 為單一劑型;其他多為最大劑量,CKD 第 3 期以上需減量;linagliptin 無腎調整。
- 優勢:體重中性、不致低血糖、廣泛適用、易用;缺點:降糖力較弱、依賴 β 細胞功能。
α-葡萄糖苷酶抑制劑|α-Glucosidase Inhibitors
- 抑制小腸刷狀緣 α-glucosidase → 碳水化合物吸收延後分布更遠端 → 降 PPG。
- 美國可用:acarbose、miglitol;其他國家:voglibose。
- 限制:每餐前服用、脹氣常見、降糖力有限;好處:不增重、不低血糖;acarbose 有 CV outcome 改善的部分證據。
- 起始:1/4 最大劑量、每日一次,數週–月內慢慢加量加頻率以提升耐受。
SGLT 抑制劑|Sodium-Glucose Transporter Inhibitors
- 機轉:腎小管葡萄糖再吸收主要由 SGLT2(高容量/低親和力,90%)負責;SGLT1(低容量/高親和力,10%)主要在腸道。家族性 SGLT2 基因突變者可日漏 170 g 葡萄糖、肥胖/糖尿病少且無腎傷害。
- 阻斷 SGLT2:降 fasting/PPG,HbA₁c ↓ 0.5–1.0%;藉糖尿伴鈉排出降 BP、減重(26 週多 2–3 kg vs placebo),改善 NAFLD(部分由減重)。
- 美國四款:canagliflozin、dapagliflozin、empagliflozin、ertugliflozin;其他:sotagliflozin(亦阻 SGLT1)。
- CV/腎益處(Table 34.10):
- EMPA-REG OUTCOME(empagliflozin、高 CV 風險 T2D):總死亡 ↓ 32%、CV 死亡 ↓ 38%、HF 住院 ↓ 35%;對既存腎疾改善。
- CANVAS(canagliflozin):CV 益處類似但較不顯著。
- DECLARE-TIMI 58(dapagliflozin):CV 死亡與 HF 住院降低。
- CREDENCE(canagliflozin、糖尿病腎病):CV 與 renal endpoint 益處。
- VERTIS-CV(ertugliflozin):未顯示同等益處。
- 一致最強的訊號為 HF 住院下降。
- 群體擴展:dapagliflozin、empagliflozin 已 FDA 批准用於有/無糖尿病的 HF;canagliflozin 限糖尿病者。CKD 保護於有/無糖尿病、有/無心臟病皆可見。
- 不良反應:
- 泌尿頻率、生殖道感染(女性 ≥ 10–15% 念珠菌感染)、UTI 偶發、脫水。
- canagliflozin 在 CVOT 增下肢截肢;其他藥物是否同樣不確定,需評估截肢史等風險因子。
- 骨質:理論顧慮、多數試驗未證實骨折增加。
- euglycemic DKA:血糖未明顯升高即可發生;可能因脫水、glucagon 上升、糖尿引起空腹下加速 gluconeogenesis;老年、代謝壓力、低碳水攝取為風險因子;持續嘔吐、噁心或不適 → 即使血糖正常仍應驗 ketones。
- Dapagliflozin 有膀胱癌警告(早期試驗膀胱癌不平衡,但其他類藥不見)。
- 啟動限制:eGFR < 45 不建議啟動降糖;對心腎益處在較低 eGFR 仍可見;需良好水分;有急性 AKI 報告。
- 機轉推測:血糖、BP、體重控制 + 體液平衡 + 抑交感 + 心肌酮體燃料增加等。
Colesevelam(膽酸結合劑)
- 第二代膽酸結合劑;T2D 中 HbA₁c ↓ ≈ 0.5%、LDL ↓ ≈ 15%、HDL 變化微;TG 可上升 5–20%(高 TG 患者避用)。
- 胃腸副作用 ≥ 10%,但少導致停藥;機轉未明。
Bromocriptine(多巴胺 agonist)
- 早晨醒後 2 小時內速釋型 bromocriptine:建立中樞多巴胺早晨高峰以改善 insulin 敏感性。
- 副作用:噁心 ≈ 30%(高劑量時 ≈ 10% 停藥);HbA₁c 下降一般輕微,最高 1.2%。1 年安全性研究 CV outcome 改善 40% vs placebo;高劑量 insulin 下血糖控制不佳者亦顯效益。但臨床採用少。
注射劑|Glucose-Lowering Agents Administered by Injection
- 多數為皮下注射;未來吸入、舌下、鼻噴等形式可能擴展(如 oral semaglutide)。教育與支持需求高於口服;筆型裝置、細針、長效藥物提升便利性。
胰島素|Insulins
- 自 1920 年代供應;T1D 必需、T2D 主流之一。皮下注射補充 basal(調肝糖製造)與 prandial(抑肝糖製造、增加肌肉/脂肪攝取)需求。
- 現多為重組人類 insulin 或合成 analog。Biosimilar 已陸續上市,FDA 標示「interchangeable」者(如 glargine-yfgn)藥師可替換。
長效 insulin|Long-Acting Insulins
- NPH(人類):起效 1–2 hr、peak 4–8 hr、duration 12–16 hr;qhs 或 BID(早餐前 + 睡前)。
- Detemir:fatty acid 共價鏈結延緩吸收與清除;duration 比 NPH 略長且更穩定;多需 BID;T2D 加 detemir 為 basal 同時口服藥可達 ≈ 40% 患者一日一次。
- Glargine U-100:酸性可溶、注射後組織中性化沉澱;多 24 hr basal effect、低 peak-to-trough 變異;低血糖風險低於 NPH;qd 早餐前或睡前。
- Glargine U-300、Degludec:qd;degludec 同時延緩吸收與清除,U-300 主要影響吸收;低血糖風險再降,特別於低劑量者與既往低血糖者。
- Icodec(研發中、未 FDA 批准):每週一次、半衰期 1 週。
短效 insulin|Short-Acting Insulins
- Regular:起效 30 min、peak 2–4 hr、duration 6–8 hr;高劑量更長。
- Lispro、Aspart、Glulisine:起效 5–15 min、peak ≈ 1 hr、duration ≈ 4 hr。
- Faster aspart (Fiasp):含 nicotinamide 加速吸收;Ultrarapid lispro (Lyumjev):含 treprostinil + citrate;皆減 PPG 但 T2D HbA₁c 改善未顯。
- U-500 regular:高度阻抗者;起效延後、作用延長;BID/TID 或 pump 使用;筆型可得;GLP1 RA 應用後使用減少。
- 吸入型 (Afrezza, Technosphere):peak 30 min、t_max ≈ 10 min(最快);duration 90–180 min;asthma/COPD 禁用;活動性肺癌、吸菸者警告;起始/6 月/年度肺功能;劑量 4/8/12 U 限制大。
預混 insulin|Premixed Insulins
- 70/30、50/50 NPH+regular;75/25、50/50 NPL+lispro;70/30 NPA+aspart;單峰 4–6 hr 後注射。
- 比 basal insulin 控糖更佳但低血糖較多。
Human vs Analog Insulin
- T1D 中 analog 益處明確;T2D 證據較弱、爭議多。Analog 低血糖較少,但 T2D 嚴重低血糖絕對風險僅 T1D 的 1/3–1/10;夜間低血糖(尤其老人)可能未察。專業 blinded CGM 與個人 CGM 在 basal-bolus 方案中可協助。Analog 列表價與自付高於 human。Allergic 反應、lipoatrophy、lipohypertrophy 罕見。
胰島素遞送裝置|Insulin Delivery Devices
- 細針/筆針更舒適;筆型 U-300 glargine 最大 160 U、U-200 degludec 大劑量適用。
- Pump:T2D 中採用低(成本效益不足);U-500 regular pump 比 TID 注射降 HbA₁c 多、用量低,但低血糖與體重無差。
- Smart pen:智慧計算、記錄;筆蓋具劑量記錄可降漏 / 重複劑量。
GLP1 受體促效劑|GLP1 Receptor Agonists
- 機轉:potentiate glucose-dependent insulin secretion、抑 PPG glucagon、延胃排空、增飽足。
- Table 34.12 清單:分短效與長效。
短效 GLP1 RA
- Exenatide (Byetta):來自 Gila monster 唾液 exendin-4,與 GLP1 53% 同源;DPP4 較不易降解。SC 後 peak ≈ 2 hr、duration < 6 hr;BID 早晚餐前 → HbA₁c ↓ ≈ 1.0%、降 PPG、減重 2–4 kg、輕度 BP/lipid 改善;惡心 ≤ 50%(多輕中度、隨時間減輕)、≈ 5% 因此停藥。腎清除:eGFR < 30 禁用。
- Lixisenatide (Adlyxin):作用稍長;qd 早餐前;降日間 PPG,夜間影響少;起始低劑量加成。
長效 GLP1 RA
- 包括 liraglutide(qd)、ER exenatide、dulaglutide、semaglutide(皆 qw);albiglutide 於美國未售;efpeglenatide 研發中。
- 比短效 HbA₁c 降幅大、空腹影響強;對 PPG 影響較小;GI 副作用較少。Semaglutide 與 dulaglutide 比,semaglutide 略勝;dulaglutide 3.0、4.5 mg、semaglutide 2.0 mg 已批准。
- 減重一致;liraglutide 3.0、semaglutide 2.4 已批准減重適應症。
- CVOT(Table 34.13):
- LEADER(liraglutide):CV composite ↓ 13%、CV 死亡 ↓ 22%、總死亡 ↓ 15%、albuminuria 進展 ↓ 26%。
- SUSTAIN-6(semaglutide):CV composite ↓ 26%、renal endpoints 下降;總死亡無差;retinopathy 進展信號(與快速降糖有關)。
- REWIND(dulaglutide)、HARMONY(albiglutide)等亦顯示益處;populations 與設計差異造成異質性。
- 短效 GLP1 RA 未顯示心血管益處。
- LEADER、SUSTAIN-6 未顯示 HF 住院降低。
- 副作用:噁心、腹瀉(短效相較 HbA₁c 下降的比例噁心更多;長效則為劑量相關);低血糖非直接效應,但合併 secretagogue 或 insulin 時應減量(secretagogue 減至最低、insulin 減 20% 除非 HbA₁c > 8%)。
- 安全性顧慮:
- 胰臟炎:postmarketing 報告、未證明因果;可能與膽石伴隨減重有關;CVOT meta 顯示 GLP1 RA 不增加,DPP4i 反而增加風險。Pancreatitis 史者避用。
- 腎:exenatide 外其他在不同 eGFR 安全;急性腎衰報告(多伴持續嘔吐、脫水、azotemia);建議若噁心、嘔吐、腹痛超過數小時,應停藥並就醫;超過 4 hr 無法保留水分需求醫。
- retinopathy:SUSTAIN-6 中 semaglutide 信號;後續 meta 顯示為快速降糖暫時性效應。
- Medullary thyroid carcinoma:人體無訊號,齧齒動物試驗有;個人或家族 MTC 史者避用。
GLP1 oral 例外
- 注射型自 2004 進入美國市場;oral semaglutide(含 SNAC 鈉鹽 N-(8-[2-hydroxybenzoyl] amino) caprylate)2019 FDA 批准;3、7、14 mg 錠,餐前 ≥ 30 min、≤ 4 oz 水、避其他藥物。劑量較大但 HbA₁c 下降與減重與其他 GLP1 RA 相當(除注射 semaglutide 外)。
GIP/GLP1 雙受體 agonist|Tirzepatide
- GIP(42 aa,小腸 K cells,受碳水化合物與脂肪刺激)增 insulin 合成/分泌、glucagon 分泌、cell proliferation;對食物攝取下降同時降惡心。早期 GIP 單獨臨床效益不彰。
- Tirzepatide 為 GLP1+GIP 受體單分子;2022 FDA 核准;vs semaglutide 1 mg:tirzepatide 5/10/15 mg 皆優;15 mg HbA₁c ↓ 2.3%(baseline 8.3%)、46% 降至 5.7%;> 10% 體重下降達 57%(vs 24%);副作用類型相似。CVOT 未完成;高價是限制。
Amylin 受體 agonist
- Amylin 與 insulin 共同分泌;T1D/T2D 皆有缺乏。促飽足、降胃排空、抑 inappropriate glucagon(葡萄糖依賴);與 insulin 協同調節血糖外觀速率。
- Pramlintide (Symlin):可溶性類比,餐前 SC;T1D/T2D 用 basal+prandial insulin 者;HbA₁c ↓ 0.5–0.7%、體重略減;mild/moderate 噁心隨時間減輕;起始 60 μg → 1–2 週內升 120 μg;mealtime insulin 減 50% 以避免低血糖;不可與需快速吸收口服藥同時(前 1 hr 或後 2 hr)。
治療的實務面向|Practical Aspects of Treatment
團隊取向|A Team Approach
- 多元決策、個別差異與時序變化使團隊照護成為必要:護理、營養、藥師、教育者、醫師(具糖尿病經驗);配合心臟、腎臟、眼科、足科次專科。
- 介入時點:診斷時、需注射或裝置時、發生重大糖尿病問題(嚴重低血糖、酮酸中毒、反覆住院)。
辨識病理生理子群|Identifying Pathophysiologic Subgroups
成人潛伏型自體免疫糖尿病|LADA
- 約 12% 成人診斷糖尿病屬於此類;β 細胞耗損常較慢、診斷常不確定。
- 常非肥胖、可能伴其他自體免疫疾病或家族史;anti-GAD 或 islet cell antibody 支持但陰性不排除。
- insulin 為主治療;早期 insulin 可能延 β 細胞功能、避高血糖暴露;SGLT2i 與 GLP1 RA 是否用於 LADA 因其 CV/腎益處仍評估中(DKA 顧慮,尤其 β 細胞耗損嚴重者)。
胰臟性糖尿病|Pancreatic Diabetes(type 3c)
- 主因:急/慢性胰臟炎、胰臟切除(癌或胰臟炎)、hemochromatosis、CF。
- 共通特徵:明顯 insulin 分泌不足、PPG 高;同時 glucagon、PP、incretin 反應均下降;可能比 T1D 血糖更不穩。
- 需 insulin(常 basal+prandial)。
單基因型糖尿病|Monogenic Diabetes
- 1–2% 新診斷成人;自體顯性、外顯率高;genetic testing 為精準醫療範例。
- GCK-MODY:β 細胞葡萄糖感應變異;輕度空腹高血糖(FPG 100–140、HbA₁c 5.6–7.8%)、不進展、無組織傷害;多在 GDM 篩檢中察覺;無需治療。
- HNF1A-MODY(最常見):成人進展性高血糖、PPG > 空腹;對 sulfonylurea 反應極佳、效益持久;HNF4α 突變亦同類反應。
標準化 vs 個別化策略|Standardized Versus Personalized Tactics
- 排除上述子群後仍稱 T2D;起始仍以標準化算法為主,再個別化。
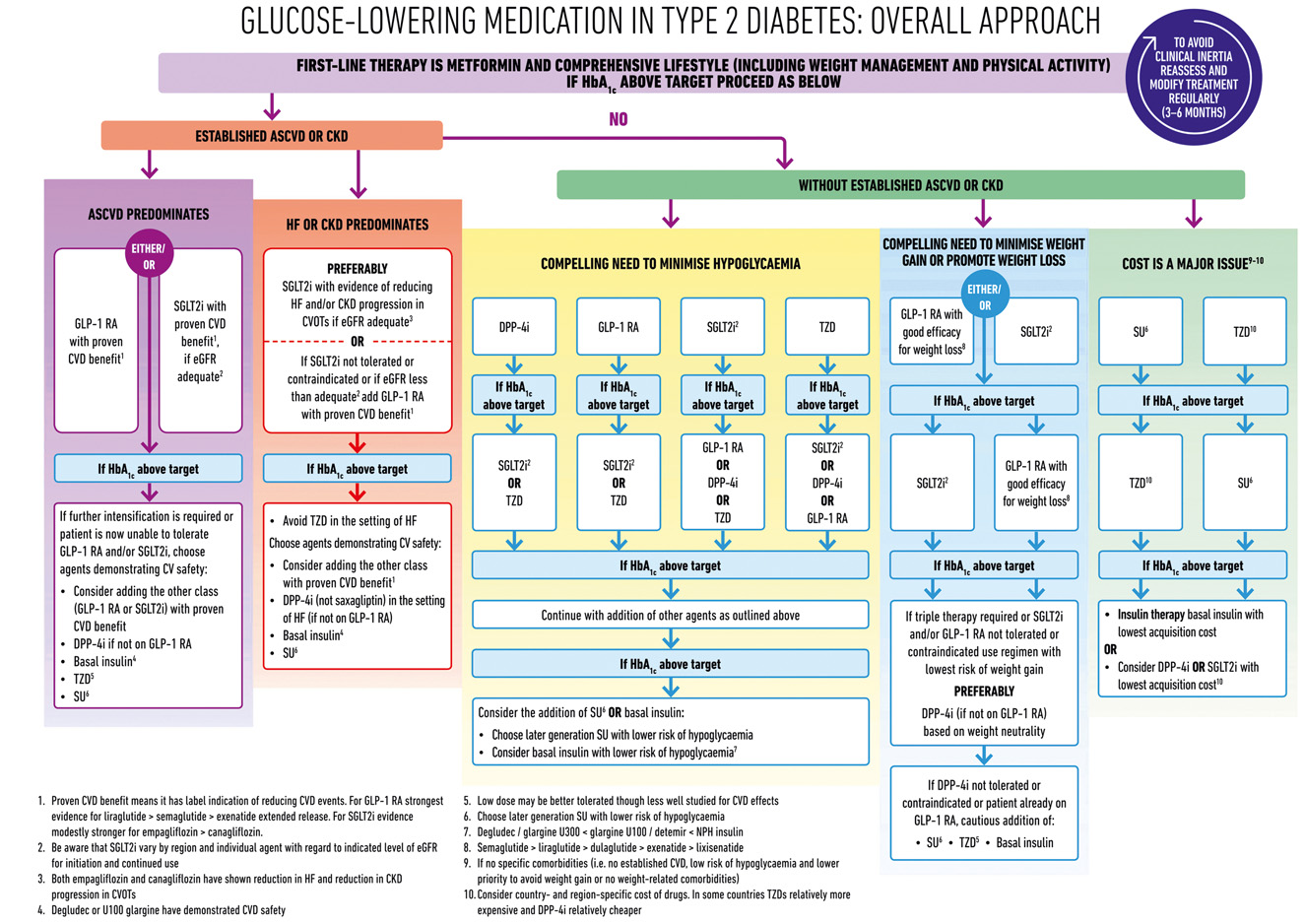
- 患者宜參與決策;指引隨 SGLT2i、GLP1 RA 證據演化(圖 34.3)。
標準化初始治療策略|A Standardized Initial Therapeutic Approach
- 長期管理核心:持續再評估血糖型態與 HbA₁c;以最簡單規格、最低劑量、最少藥物達成最佳控制。
- 5 年後多數需 ≥ 2 種藥物;早期傾向加藥而非取代。
Metformin
- 一般考量為腎功能足夠 T2D 之首選 + diet/exercise/DSMES。
- 可用於糖尿病前期延緩進展;HbA₁c < 6.5% 仍可繼續;CV 益處與 SGLT2i、GLP1 RA 類似可能要多年才顯現。
- 已知 ASCVD/CKD 者,是否以 SGLT2i/GLP1 RA 為一線仍有爭議;多數患者診斷時尚無這些併發症。
- 不耐或禁忌或 3–6 個月內反應不足 → 取代或加:SGLT2i、GLP1 RA、SU、TZD、DPP4i、basal insulin、tirzepatide。雙藥(metformin + 任一)多可維持目標 5–10 年。
階梯式合併治療:口服藥或 basal insulin|Stepwise Combination Therapy
- 主流組合作用相加;半最大劑量已可達 > 一半最大效果且副作用較少。
- 例:metformin 500 mg BID + glimepiride 1 mg/d 多優於單藥滿劑量;若 metformin 已 2000 mg 且良好耐受,加第二藥不需減 metformin(除非腎功能下降)。
- basal insulin 加入時可繼續 metformin、SU 以維持控糖、降 insulin 劑量與低血糖風險。
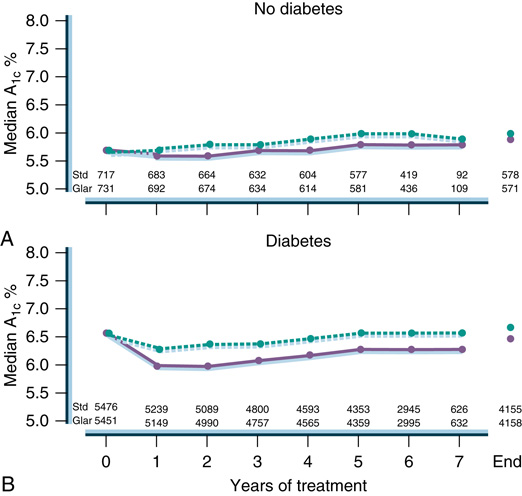
- ORIGIN trial(圖 34.4):dysglycemia 或新 T2D + 高 CV 風險;隨機 glargine 為主 vs 漸進口服藥;雙組 5 年內維持 HbA₁c ≈ 6.5%;除 glargine 組低血糖較多、進展糖尿病較少外無 outcome 差異。
- GRADE study(5047 人,Black ≈ 20%、Hispanic ≈ 20%;HbA₁c 6.8–8.5%):metformin 加 glimepiride、glargine、sitagliptin、liraglutide。
- HbA₁c < 7% 維持時間:liraglutide ≈ glargine > glimepiride ≈ sitagliptin;sitagliptin 在 HbA₁c ≥ 7.8% 最弱。
- liraglutide GI 副作用較多,整體 AE 相近;嚴重低血糖以 glimepiride 較多。
- 體重增加:glimepiride、glargine 較多。
- 微血管 outcome 無差別;SGLT2i 未納入。
治療個別化考量|Considerations in Personalizing Therapy
- 任何類別藥物均可能成為第二線;理由與選擇應與患者討論。
Sulfonylurea 以外的口服藥與非 insulin 注射劑|Oral Agents Beyond Sulfonylureas and Injected Therapies Other Than Insulin
- DPP4i、TZD(pioglitazone)、長效 GLP1 RA 常與 metformin 合併。
- DPP4i 降糖力小於 SU 但低血糖少、症狀少;fixed-dose combo 簡化處方。
- Pioglitazone 變異大、可增重水腫,但改善周邊敏感性、降肝脂;NASH 多以 45 mg 研究,常處方較低劑量。
- GLP1 RA 注射型在 GRADE 與 basal insulin 等效;qw 長效 GLP1 RA 一般優於 liraglutide。減重、低低血糖;高 CV 風險者優於 insulin。GI 為主要副作用;qw 提升便利與依從。Oral semaglutide 為替代選項。
- 啟動 GLP1 RA 時應停 DPP4i(機轉相似)。
- Basal insulin + GLP1 RA 固定組合可作初始注射;劑量選擇與滴定需專業。
- ASCVD(尤其 HF)患者:早用 SGLT2i;其降糖力中等。
Basal Insulin
- 唯一必須個別化的類別;生理與行為皆驅動;basal insulin 失效後再 basal-bolus 為標準;clinical inertia 是延遲加藥的主因。
- 劑量範圍 10–200 U/d;起始 10 U 或 0.1–0.2 U/kg;以 SMBG/CGM 早餐前血糖為標的滴定(每週 2–4 U 或每日 1 U)。
- 多數需 0.4–0.5 U/kg;初期 fasting 目標 ≤ 100 mg/dL 多可達且低血糖少;HbA₁c > 8% 開始者初目標 < 120 mg/dL 較安全。
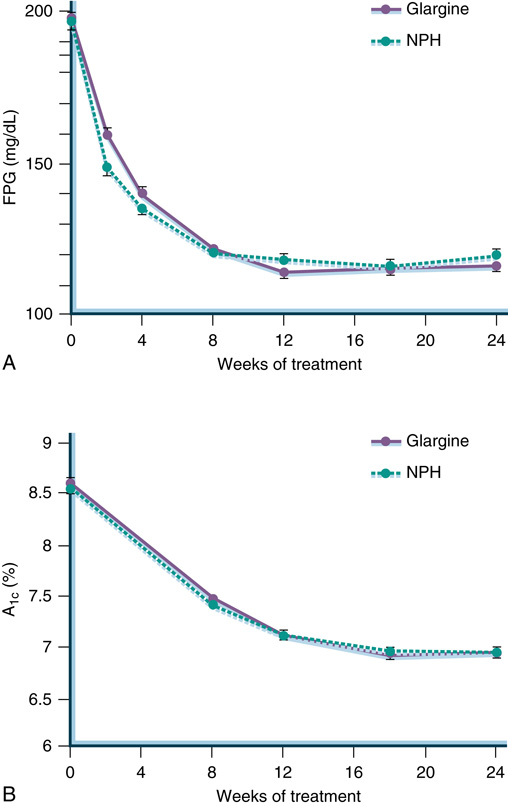
- patient-directed titration 安全有效;圖 34.5 NPH vs glargine 在 1–2 oral agent 下加 basal 的反應;12 週後 fasting 多穩定,HbA₁c 略落後。
- HbA₁c 仍未達目標即使 basal 妥善滴定 → 處理 PPG。
處理餐後高血糖|Treating Postprandial Hyperglycemia
- 未治療 T2D 高血糖暴露多源於 basal 而非 PPG,HbA₁c > 8.0% 時尤明顯。
- 多數降糖藥對 basal 強於 PPG;初期介入後殘餘暴露多為 PPG;β 細胞功能下降後 PPG 漸升、HbA₁c 維持目標漸難。
- 早餐後 PPG 增最大;最高 PPG 出現於晚餐後。10 年後常需個別化的 PPG 治療。
- 飲食策略:少量多餐、選擇低 GI、低快速吸收食物。
- 短效 secretagogue:多次日小劑量降 PPG。
- AGI 對 PPG 顯著有效但 GI 副作用限制。
- 短效 insulin(最有效):1 餐 4 U 或 10% basal 起步;12 週內 1–2 U 或 10–15% 雙週滴定,目標前一餐前血糖近 120(80–130);總日劑量常需 > 1 U/kg;basal 通常不分二劑;CGM 適用於 ≥ 3 注射/d。
- 取代/補強:以 GLP1 RA 加 basal 而非加 prandial insulin 為偏好(除非已使用 GLP1 RA);短效 GLP1 RA 對 PPG 較強,但長效仍可能與加 prandial insulin 的整體效力相近,並少低血糖、少體重增加。
- 「Overbasalization」:HbA₁c < 8% 仍持續加 basal → 夜間低血糖;加新藥時 basal 降量為宜。
治療個別化選擇實例|Examples of Personalized Choices of Therapy
心血管風險最低化|Minimizing Cardiovascular Risks
- Metformin 為基礎(CV 益處可能多年顯現);2008 年起 CVOT 要求帶來 GLP1 RA 與 SGLT2i 的明確 CV 益處(已知 ASCVD 或極高風險者)。
- 對既有 ASCVD(無 HF):兩類皆可;GLP1 RA HbA₁c 下降較多、可能對 stroke 與 MALE 有獨特益處。
- 對 HF(特別 HFrEF):SGLT2i 為首選。
減緩腎病進展|Reducing Progression of Kidney Disease
- T2D 30–40% 有 CKD;ESRD 全球持續上升。
- ACEi/ARB 為基礎;finerenone(MR antagonist)可延腎功能下降。
- SGLT2i 顯示最大益處:albuminuria、Cr 加倍、40% eGFR 下降、ESRD、死亡之 composite 改善 30–50%;於 CKD 不論糖尿病有無皆顯效益;雖降糖力隨 eGFR 下降,CV/腎益處跨 baseline eGFR 維持。
- GLP1 RA 也有腎益處但程度小於 SGLT2i。
低血糖最少化|Minimizing Hypoglycemia
- 老人、長期糖尿病、認知功能下降、腎病 → 跌倒、傷害風險高;恐懼低血糖造成 inertia 與依從不佳;嚴重低血糖史為強風險因子。
- 低風險選項:metformin 單用、DPP4i、GLP1 RA、SGLT2i、GIP/GLP1 dual、TZD。需 insulin 時新型長效降風險最低;嚴重低血糖史可放寬 HbA₁c 目標至 7–8% 或更高。
體重增加最少化|Minimizing Weight Gain
- 強調 diet/exercise + metformin;二線可選 GLP1 RA、GIP/GLP1 dual、SGLT2i。
- 減重排序(藥物):tirzepatide > 長效 GLP1 RA(特別 semaglutide)> SGLT2i。
- 減重手術益處可能大於藥物(見 Ch40),但超出本章範圍。
- SU、pioglitazone、prandial insulin 因增重而不優先;basal insulin 比 prandial 增重少。
成本最少化|Minimizing Costs
- 對開發中國家或保險不足者,藥費限制是治療成敗關鍵。
- 最便宜:metformin、SU、pioglitazone、AGI、human insulin。
- 美國 ReliOn 為品牌 human regular/NPH/70-30,list price ≈ analog 的 10%;human insulin 治療 T2D 仍可行但需 BID NPH、固定餐次、HbA₁c 目標可放寬至 7.5–8.0% 以避低血糖。WHO 對低資源環境採此原則。
臨床管理特殊狀況|Special Situations in Clinical Management
診斷時嚴重高血糖|Severe Hyperglycemia at Diagnosis
- 嚴重脫水、酸中毒、心智改變、共病重 → 入院 IV 液體 + insulin;部分恢復者經治療後可僅靠生活型態維持,可能屬 ketosis-prone diabetes。
- HbA₁c > 10%、隨機血糖 > 300 或具 catabolic 症狀但無酸中毒:注意是否大量含糖飲料;多數建議起始 insulin。2–4 週積極降糖達近正常後,HbA₁c < 6.5–7% 可維持 ≥ 1 年(即使停藥);可作為「逆轉 glucolipotoxicity」proof of principle,但未普及為標準。
- 高 HbA₁c 者亦可雙/三藥起步(含 basal insulin);單藥+多藥比達標一致性與耐久性更佳。
- 急診 SU 起步亦顯效益;GLP1 RA 雖長期有用但 GI 與緩慢滴定使其在重度高血糖起步較不理想。
- HbA₁c > 9% 且有 retinopathy → 6 個月內漸降至 < 7%(避免快降致 retinopathy/PN 惡化);其後至少維持 metformin。
兒童與青少年 T2D|Type 2 Diabetes in Youth
- 隨肥胖增加,少於 20 歲發病增多(弱勢族裔顯著);某些區域兒童 T2D 接近 T1D 發生率。
- 病理:嚴重 insulin 阻抗 + 初期高 insulin 分泌 → β 細胞功能快速下降,metformin 無法延緩。
- 強調飲食/運動,家庭參與;多數目標 HbA₁c < 7%。
- 起始:metformin;FPG > 250 或 HbA₁c > 8.5% → 加 basal insulin;酸中毒或重症狀 → basal-bolus。
- liraglutide ≥ 10 歲已批准 add-on;qw GLP1 RA 在此族群尚 off-label。
- 早期成年期併發症風險高,應從一開始注重併發症預防。
妊娠|Pregnancy
- 詳細管理見其他章節。GD 後 50–70% 在 15–25 年內出現 T2D(風險增 10–18×);定期 1–3 年驗血糖/HbA₁c。
- GD 對母嬰皆有立即風險(複雜分娩、新生兒併發症);子代日後肥胖/T2D 風險上升,可由良好血糖控制減弱。
- 育齡 T2D 婦女:preconception planning(妊娠前 10 週控糖以降胎兒畸形);目標 fasting < 95、1-hr PPG < 140、2-hr PPG < 120、HbA₁c < 6.0%。
- 主要 insulin;metformin 與 sulfonylurea(glyburide)有時使用但安全性疑慮(SU 尤甚);既存 T2D 多建議 insulin。
第 2 型糖尿病的預防|Preventing Type 2 Diabetes Mellitus
- 隨機試驗:生活型態介入降進展風險 30–60%(3–5 年),效益持久且與減重相關(平均 ≈ 5%)。
- Metformin 預防效力較小,但對 < 60 歲、BMI ≥ 35、FPG ≥ 110、HbA₁c ≥ 6.0%、過去 GD 者效益接近生活型態介入;> 60 歲或 BMI < 30、FPG < 100 者效益小;持久且具成本效益。
- Acarbose 亦降進展,無亞群差異;TZD 改善阻抗、可延 onset,但長期心、骨副作用限制使用。GLP1 RA 有潛力但成本與初期副作用限制。減重手術降低重度肥胖者進展。
- 篩檢與生活型態介入是最佳投資;CDC National Diabetes Prevention Program 為現行公衛框架(22 場結構化課程,群體或線上);提供認證機構標準化執行。
- 藥物預防地位較不明確(短期內進展至顯著併發症的時間窗有限);對特定高風險族群(BMI ≥ 35、< 60 歲、過去 GD)建議考量 metformin。
未來方向|Future Directions
- 現代 T2D 治療比過往更有效且更易執行:飲食原則、降糖藥減重、減頻、避低血糖、降 CV/腎併發症。
- 研發中:β 細胞 glucose-dependent insulin 分泌、incretin 軸調節、肝糖製造調節、insulin 敏感性增強。
- Glucokinase activator:增 insulin 分泌、可能肝毒性與低血糖;探索低劑量、β 細胞特異性。
- Dual/triple agonists:tirzepatide 已上市;GLP1-glucagon dual、GLP1-GIP-glucagon triple、oxyntomodulin(GLP1+glucagon dual)等於開發中。
- Adiponectin pathway、Imeglimin(兼增分泌與肌肉敏感性)、glucose-responsive insulin(單注射涵蓋 basal 與 prandial)。
- Smart 監控、便利給藥工具持續演進。
- 主要瓶頸非工具不足而是經濟、心理、組織障礙;公衛策略、篩檢效率、全球醫療公平仍待加強。
—— 本章結束 ——
TEACHING SLIDES
Williams Endocrinology 15e Ch34|第 2 型糖尿病的治療
01 全球與經濟負擔
- T2D 佔全球糖尿病 ≈ 90%
- IDF 2021 5.36 億 → 2045 推估 7.83 億
- 美國 11.3% 糖尿病、38% 糖尿病前期
- 2017 美國直接醫療支出 3,270 億 USD
- 美國併發症 1990–2010 ↓ 50%,但 ESRD 又上升
02 診斷標準
- FPG ≥ 126 mg/dL(7.0 mmol/L)
- 2-hr PG ≥ 200 mg/dL(11.1 mmol/L)
- HbA₁c ≥ 6.5%(48 mmol/mol)
- 隨機 ≥ 200 + 典型症狀
- HbA₁c CV < 2% 比 FPG/2-hr PG 穩定
03 篩檢族群(ADA Box 34.1)
- BMI ≥ 25(亞洲 ≥ 23)+ 風險因子
- 一等親糖尿病
- 高風險族裔、CVD、HTN、低 HDL、高 TG
- PCOS、不活動、acanthosis nigricans
- 糖尿病前期年檢、GDM 史每 ≥ 3 年、其餘 45 歲開始
04 介入研究關鍵訊息
- UKPDS:SU/insulin 微血管 ↓ 25%;20 年 MI ↓ 15%、總死亡 ↓ 13%
- UKPDS:metformin(過重)MI ↓ 39%、總死亡 ↓ 36%
- ACCORD:HbA₁c < 6% → 總死亡 ↑ 22%
- 死亡集中於目標 < 6% 但無法降至 < 7% 者
- 「Legacy effect」:早期良好控制效益持久
05 ADA 血糖目標
- HbA₁c 一般 < 7%;高風險 7–8%
- 餐前 80–130 mg/dL(4.4–7.2)
- 餐後峰值 < 180(10.0)
- ACE:HbA₁c ≤ 6.5%、餐後 < 140
- 目標需個別化
06 監測工具與低血糖三級
- HbA₁c 反映 2–3 個月平均
- SMBG:T1D、強化 insulin、新診斷
- CGM:T2D + insulin、虛擬照護、Medicare 已給付
- L1 < 70(警示)、L2 ≤ 54(顯著)、L3 需協助
- 「Glycation gap」≥ 0.3–0.4% 應辨識
07 DSMES 與 MNT
- DSMES 降 HbA₁c 0.45–0.57%
- 7 要件、四關鍵時點、使用率 ≤ 7%
- MNT 6 個月 3–6 次,HbA₁c ↓ 0.3–2.0%
- 減重 5% → 代謝益處;> 15% → 86% HbA₁c < 6.5%
- 巨量營養素分布 < 總熱量降低重要
08 Metformin
- 首選、HbA₁c ↓ 1.0–2.0%
- 機轉:AMPK、抑 mGPDH、腸道效應、↑ GLP1
- eGFR < 45 不啟動、< 30 禁用
- vit B₁₂ 缺乏可補 1000 μg/d
- UKPDS:MI ↓ 39%、總死亡 ↓ 36%
09 Sulfonylurea
- HbA₁c ↓ 0.5–1.5%;SUR1/KATP
- glimepiride、ER glipizide、ER gliclazide 首選
- glyburide 低血糖最高、SUR2 影響 ischemic preconditioning
- 起始低劑量(如 glimepiride 0.5–1 mg)
- CAROLINA:glimepiride MACE = linagliptin
10 TZD(pioglitazone, rosiglitazone)
- PPARγ;HbA₁c ↓ 0.75–1.5%
- 改善 insulin 阻抗、降 FFA
- pioglitazone:NASH 改善、stroke 後再事件 ↓
- 副作用:增重、水腫、HF、骨折(女性遠端)
- 膀胱癌史 → 避 pioglitazone
11 DPP4 inhibitor
- 內生 GLP1 ↑ ≈ 2×
- HbA₁c ↓ 0.5–1.0%
- 體重中性、低血糖少
- saxagliptin/alogliptin 增 HF 住院;sitagliptin 無
- linagliptin 不需 eGFR 調整
12 SGLT2 inhibitor
- HbA₁c ↓ 0.5–1.0%、減重 2–3 kg、降 BP
- EMPA-REG:CV 死亡 ↓ 38%、HF 住院 ↓ 35%
- HF(有/無 DM)與 CKD 益處跨越糖尿病
- 副作用:生殖部位黴菌、UTI、euglycemic DKA
- canagliflozin 截肢、dapagliflozin 膀胱癌警告
13 α-GI、Colesevelam、Bromocriptine
- AGI(acarbose、miglitol、voglibose):PPG、不低血糖、脹氣
- acarbose 有部分 CV 益處
- Colesevelam:HbA₁c ↓ 0.5%、LDL ↓ 15%、TG ↑ 5–20%
- Bromocriptine(quick-release):早晨服用、噁心常見
- 兩者目前少用
14 Insulins(Long-acting)
- NPH:peak 4–8 hr、duration 12–16 hr
- detemir:較穩定、可 qd 或 BID
- glargine U-100:> 24 hr、低 peak
- glargine U-300、degludec:再降低血糖
- icodec(研發中):每週一次
15 Insulins(Short-acting)
- Regular:30 min、4–8 hr
- Lispro/Aspart/Glulisine:5–15 min、≈ 4 hr
- Faster aspart (Fiasp)、Lyumjev:吸收更快
- 吸入 Afrezza:peak 30 min;asthma/COPD 禁用
- U-500:嚴重阻抗
16 Premixed 與 Human vs Analog
- 70/30 等:方便但低血糖較多
- T1D 中 analog 益處明確
- T2D 中 analog 低血糖較少但價格高
- 嚴重低血糖絕對風險為 T1D 的 1/3–1/10
- ReliOn human insulin ≈ analog 10% 價格
17 GLP1 RA 概論
- 短效:exenatide、lixisenatide
- 長效:liraglutide、ER exenatide、dulaglutide、semaglutide
- 短效 PPG 強、長效 basal 強且 GI 較輕
- HbA₁c ↓ 1.0–1.8%、減重 2–10 kg
- liraglutide 3.0、semaglutide 2.4 已批准減重
18 GLP1 RA CVOT
- LEADER(liraglutide):CV death ↓ 22%
- SUSTAIN-6(semaglutide):CV composite ↓ 26%
- 短效藥物未顯示 CV 益處
- 多無 HF 住院顯著下降
- 警示:MTC 史避用、SUSTAIN-6 retinopathy 訊號
19 Tirzepatide(GIP/GLP1)
- HbA₁c ↓ 2.3%(15 mg;baseline 8.3%)
- 46% 降至 5.7%
-
10% 體重下降達 57%(vs semaglutide 1 mg 24%)
- CVOT 尚未完成
- Pramlintide:amylin 類比、+prandial insulin
20 標準化起始策略
- Metformin(除非禁忌)+ DSMES
- 3–6 個月未達標 → 加第二線
- 第二線:SGLT2i、GLP1 RA、SU、TZD、DPP4i、basal insulin
- ASCVD/HF/CKD:早用 SGLT2i / GLP1 RA
- GRADE:liraglutide ≈ glargine > glimepiride ≈ sitagliptin
21 Basal insulin 滴定
- 起始 10 U 或 0.1–0.2 U/kg
- 早餐前 SMBG 為標的
- 多數需 0.4–0.5 U/kg
- 起始 fasting 目標 ≤ 100;HbA₁c > 8% → < 120
- 12 週後 fasting 多穩定
22 PPG 處理
-
8% 主要為 basal 過剩
- 殘餘暴露 PPG 隨 β 細胞下降增加
- AGI、短效 secretagogue、prandial insulin
- 加 GLP1 RA 比加 prandial insulin 多優(少低血糖、少增重)
- 注意 overbasalization
23 個別化目標
- 心血管:metformin + SGLT2i / GLP1 RA
- HF:SGLT2i 首選
- CKD:SGLT2i > GLP1 RA(finerenone 加成)
- 低血糖最少化:DPP4i、GLP1 RA、SGLT2i、TZD
- 體重:tirzepatide > GLP1 RA > SGLT2i
24 病理生理子群
- LADA:≈ 12% 成年發病;anti-GAD 陽性提示
- 胰臟性糖尿病(type 3c):胰臟炎、CF、hemochromatosis
- GCK-MODY:輕度穩定空腹高血糖、不需治療
- HNF1A-MODY:對 SU 反應極佳
- 10–19 歲非歐裔 T2D 快速上升
25 特殊狀況
- 嚴重高血糖呈現:HbA₁c > 10% → 多建議 insulin
- HbA₁c > 9% + retinopathy → 6 個月內漸降 < 7%
- Youth-onset:β 細胞快速下降;FPG > 250 或 HbA₁c > 8.5% 加 basal insulin
- Pregnancy:fasting < 95、1-hr < 140、2-hr < 120、HbA₁c < 6.0%
- 主要使用 insulin;metformin/glyburide 安全性有疑慮
26 T2D 預防
- 生活型態介入:進展風險 ↓ 30–60%
- Metformin:< 60 歲、BMI ≥ 35、過去 GD 等效益接近生活型態
- Acarbose:亦降進展,無亞群差異
- 減重手術:重度肥胖者降進展
- CDC National DPP 為現行公衛框架
27 未來方向
- 雙/三激素 agonists(GLP1-glucagon、GIP-GLP1-glucagon)
- Glucokinase activator:β 細胞特異性開發
- Imeglimin:兼增分泌與肌肉敏感性
- Glucose-responsive insulin(basal+prandial 單注射)
- 公衛、組織、成本仍是主要瓶頸