胰島素阻抗的錯誤迷思
解迷思
名詞釋義:
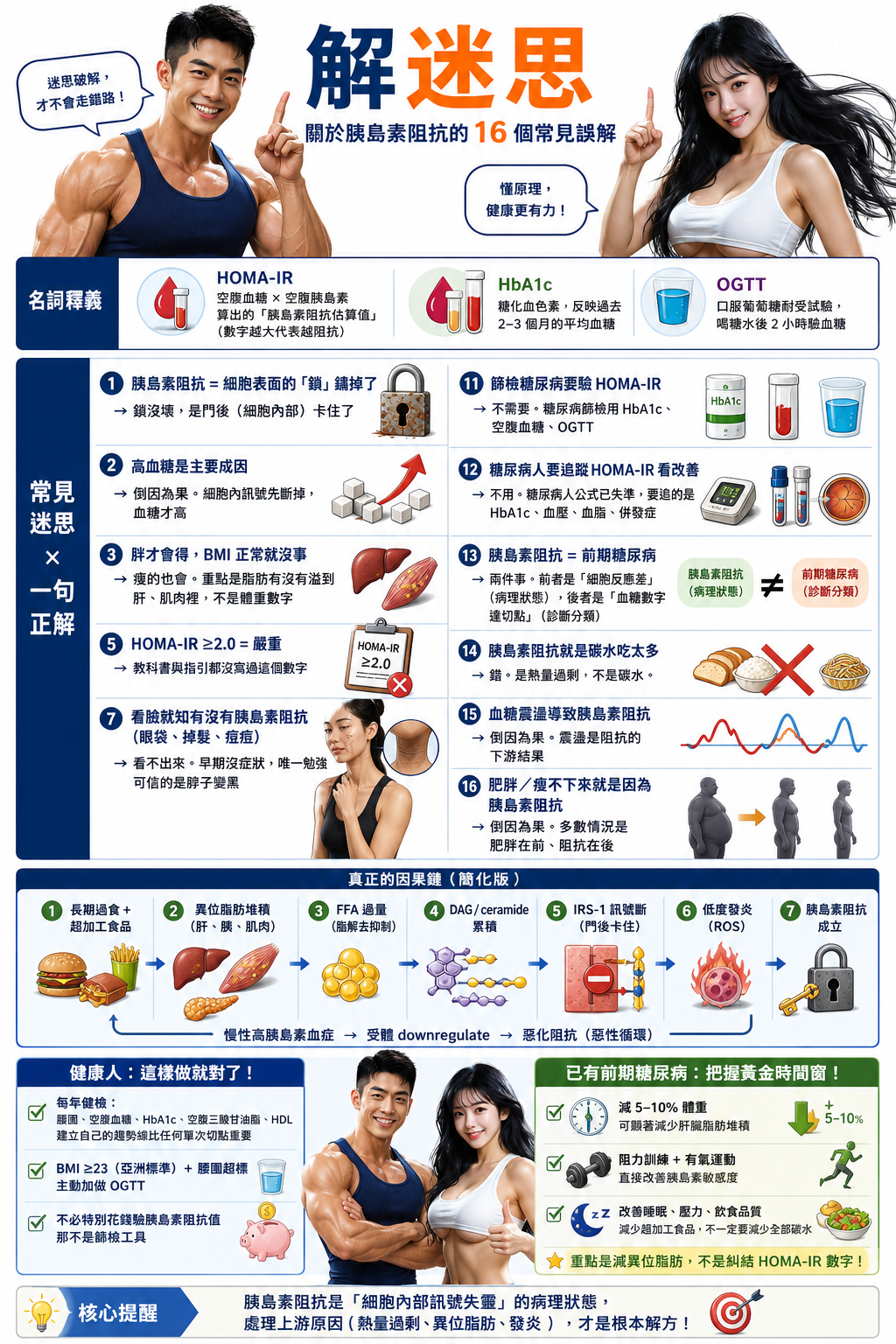
- HOMA-IR = 空腹血糖 × 空腹胰島素算出的「胰島素阻抗估算值」(數字越大代表越阻抗)
- HbA1c = 糖化血色素,反映過去 2–3 個月的平均血糖
- OGTT = 口服葡萄糖耐受試驗,喝糖水後 2 小時驗血糖
| 常見迷思 | 一句正解 |
|---|---|
| 1. 胰島素阻抗 = 細胞表面的「鎖」鏽掉了 | 鎖沒壞,是門後(細胞內部)卡住了 |
| 2. 高血糖是主要成因 | 倒因為果。細胞內訊號先斷掉,血糖才高 |
| 3. 胖才會得,BMI 正常就沒事 | 瘦的也會。重點是脂肪有沒有溢到肝、肌肉裡,不是體重數字 |
| 5. HOMA-IR ≥2.0 = 嚴重 | 教科書與指引都沒寫過這個數字 |
| 7. 看臉就知有沒有胰島素阻抗(眼袋、掉髮、痘痘) | 看不出來。早期沒症狀,唯一勉強可信的是脖子變黑 |
| 11. 篩檢糖尿病要驗 HOMA-IR | 不需要。糖尿病篩檢用 HbA1c、空腹血糖、OGTT |
| 12. 糖尿病人要追蹤 HOMA-IR 看改善 | 不用。糖尿病人公式已失準,要追的是 HbA1c、血壓、血脂、併發症 |
| 13. 胰島素阻抗 = 前期糖尿病 | 兩件事。前者是「細胞反應差」(病理狀態),後者是「血糖數字達切點」(診斷分類) |
| 14. 胰島素阻抗就是碳水吃太多 | 錯。是熱量過剩,不是碳水。 |
| 15. 血糖震盪導致胰島素阻抗 | 倒因為果。震盪是阻抗的下游結果 |
| 16. 肥胖/瘦不下來就是因為胰島素阻抗 | 倒因為果。多數情況是肥胖在前、阻抗在後 |
詳解:逐條訂正
1. 「鎖鏽掉」不是真相 — 是門後被卡住
「胰島素是鑰匙、細胞是鎖、阻抗就是鎖鏽掉了」這比喻 1990 年代很紅,2025 年來看是錯的。
胰島素跟受體的結合本身好好的。問題出在受體之後、細胞內部那一整段訊號鏈:胰島素受體自磷酸化 → IRS-1 → PI3K → AKT → GLUT4 移到細胞膜(讓葡萄糖進來)。
肌肉、肝臟細胞內若堆積太多脂質中間產物(DAG 與 ceramide),這些垃圾會活化 novel PKC,把 IRS-1 上的 serine 殘基磷酸化 — 等於把門卡死。鎖好好的,鑰匙照按,但門就是打不開。
連基因層面也是這樣:第一個被找到的第 2 型糖尿病風險變異就是 IRS-1 上的 Gly972Arg,影響的是 PI3K,不是受體。
2. 高血糖不是「主要成因」 — 是下游結果
「血糖一直高,細胞被高糖泡到變鈍」。教科書沒這樣寫。
Harrison 內科學代謝症候群章直接點明:胰島素阻抗的核心是「受體後 (post-receptor) 訊號失靈」,受體本身的變化(如骨骼肌受體濃度與酪胺酸激酶活性下降)極可能是高胰島素血症的繼發結果,不是原發缺陷。
順序大致是:
- 長期過食 + 超加工食品 → 異位脂肪堆積(肝、胰、肌)
- 細胞內 DAG / ceramide 把 IRS-1 訊號切斷
- 訊號斷 → 葡萄糖進不去肌肉 → 血糖才在血液裡堆高
- 胰臟代償性分泌更多胰島素 → 慢性高胰島素血症 → 受體進一步 downregulate
對正常人連續 24 / 72 小時維持高胰島素,葡萄糖處置力就會被特異性壓低;反過來,肥胖、阻抗病人若把胰島素分泌壓下來,敏感度反而回升。
對病人意義:只想著「降血糖」是處理下游。要動的是上游 — 異位脂肪 + 熱量盈餘 + 超加工食品。
3. 「胖才會得」是錯的 — 是個人脂肪閾值
每個人皮下脂肪倉庫的容量不一樣。倉庫大的人可以胖到 BMI 35 還沒事;倉庫小的 BMI 23 就爆倉。爆倉的脂肪溢到肝、胰、肌肉內部 — 異位脂肪 (ectopic fat) 才是真正的引擎。
東亞人天生倉庫偏小、胰臟代償力較弱。這就是為什麼 ADA 2026 §2 把亞裔的篩檢 BMI 切點下修到 ≥23,不是西方的 ≥25。
「我 BMI 才 23,沒事」的長輩,腰圍超標、家族史強,該查還是要查。
5. HOMA-IR ≥2 是嚴重?
「HOMA-IR ≤1.4 正常、1.5–1.9 輕微、≥2.0 嚴重」是中文衛教與健檢診所最愛引的數字組合。
問題是:本文所引用的教科書或臨床指引,全部沒寫過這個切點。
7. 看臉看不出胰島素阻抗
Harrison 內科學教科書的篩檢風險因子表裡,唯一被列為皮膚線索的是黑色棘皮症 (acanthosis nigricans),且明文寫「列為篩檢指標,不是診斷標準」。
11. 篩檢糖尿病要驗「胰島素阻抗」?
驗胰島素阻抗並不是糖尿病篩檢的標準工具。
ADA 2026 §2 Recommendation 2.13 + Table 2.5 寫得很清楚:糖尿病風險篩檢用 HbA1c、空腹血糖、OGTT;風險因子(家族史、肥胖、PCOS、亞裔 BMI ≥23 等)決定誰要做這三項。HOMA-IR 與空腹胰島素不在篩檢流程內。台灣糖尿病臨床指引也沒把 HOMA-IR 列入篩檢流程。
胰島素阻抗是病理生理狀態,不是糖尿病的判準。把驗胰島素當篩檢,是把研究工具誤用到臨床路徑上。
12. 糖尿病人應該追蹤「胰島素阻抗值」?
「糖尿病確診了,每三個月驗一次 HOMA-IR 看有沒有改善」。沒有指引建議這樣做。
糖尿病人的標準追蹤目標是:HbA1c(血糖控制)、血壓 / 血脂 / 腰圍(共病)、併發症監控(眼底、神經、蛋白尿、心血管)。這些有 hard outcome 或試驗實證支持。
HOMA-IR 在糖尿病人身上還會技術性失準:公式假設 β 細胞還能代償,但糖尿病人多數 β 細胞功能已部分喪失,計算結果解讀不易。
「我的 HOMA-IR 從 4 降到 2」可能只是 β 細胞分泌力下降,不代表敏感度真的回升。
13. 胰島素阻抗 = 前期糖尿病?
這是兩個不同層次的概念:
| 胰島素阻抗 | 前期糖尿病 | |
|---|---|---|
| 性質 | 病理生理狀態(細胞對胰島素反應變差) | 診斷分類(血糖數字達某切點) |
| 怎麼定義 | 沒有單一臨床切點 | HbA1c 5.7–6.4% 或空腹血糖 100–125 mg/dL 或 OGTT 2 小時 140–199 mg/dL |
| 可不可以阻抗高但血糖正常 | 可以(早期、β 細胞代償強) | 該情況不算前期糖尿病 |
| 可不可以前期糖尿病但阻抗不嚴重 | 可以(β 細胞先衰退為主,東亞較常見) | – |
兩個高度相關但不等同。前期糖尿病有正式的切點與處置建議,胰島素阻抗沒有。把兩者畫等號會誤導:阻抗高的人以為自己已經前期糖尿病而過度焦慮,或前期糖尿病的人以為「阻抗值正常」就沒事。
14. 胰島素阻抗就是「碳水吃太多」?
低碳水化合物 / 生酮飲食社群把胰島素阻抗的成因簡化成「碳水/糖吃太多」。這是中文社群最深植、流傳最廣的錯誤模型 — 也最嚴重,因為它把治療方向帶偏。
真正的因果鏈:
- 長期熱量過剩 + 超加工食品(不論碳水、脂肪、酒精)→ 皮下脂肪倉庫達到個人閾值 → 多餘脂肪溢出
- 脂肪溢出沉積到肝臟、胰臟、肌肉細胞內 → 異位脂肪 (ectopic fat)
- 循環中游離脂肪酸 (FFA) 過量:脂肪組織脂解 + 脂蛋白脂解酵素持續產生 FFA。胰島素本來在脂肪組織抑制脂解,是它最敏感的作用之一;阻抗一形成,脂解去抑制 → FFA 上升 → 削弱胰島素抗脂解力 → 惡性循環
- 異位脂肪在肌肉與肝細胞內代謝產生 DAG(雙酸甘油酯)與 ceramide(神經醯胺)
- 這些脂質中間產物活化 novel PKC、mTOR/S6K,把 IRS-1 上的 serine 殘基磷酸化 — 訊號鏈當場被切斷
- 受損的脂肪酸氧化作用 + 細胞內脂質堆積 → 產生反應性氧化物(ROS)→ 低度代謝性發炎 (low-grade metabolic inflammation) → 透過回饋機制再惡化阻抗
- 胰島素還在分泌、受體還在結合,但細胞內已經收不到訊號 → 阻抗成立
整條因果鏈的核心是 「異位脂肪 → FFA 過量 → 細胞內脂質中間產物 → 訊號切斷 + 低度發炎正回饋」,不是碳水攝取本身。
| 錯誤信念 | 實情 |
|---|---|
| 「胰島素是脂肪儲存的開關 → 少碳水 → 少胰島素 → 不胖 → 阻抗改善」 | 高胰島素血症的因有很多,過食與肝臟清除率下降是主軸;單壓碳水不能解決 |
| 「低碳就是胰島素阻抗的解方」 | 減重才是;低碳是減重工具之一,地中海飲食也是。 |
| 「不吃碳水血糖就不會震盪,阻抗就不會惡化」 | 短期血糖看起來穩 ≠ 異位脂肪移除;脂肪不退,敏感度不會回 |
真正能改善胰島素阻抗的做法:
- 熱量赤字 + 食物品質提升(減少超加工食品、不一定減少全部碳水)
- 規律運動(透過 AMPK 路徑直接拉走肌肉內脂質;運動降血糖與胰島素訊號完全獨立)
- 體重下降 5–10% 即可顯著減少肝臟脂肪堆積
- 改善睡眠、壓力、戒菸
實用建議:「你不是該戒碳水,你是該把異位脂肪移走」。可達到後者的方法不只一條;低碳是其中一條,未必最好走。
15. 血糖震盪 → 胰島素噴發 → 引發胰島素阻抗?
連續血糖監測(CGM)近年大紅,社群與生酮 KOL 大量推銷「血糖震盪導致胰島素阻抗」這個假說:吃碳水血糖飆 → 胰島素噴發 → 血糖驟降 → 飢餓再吃 → 阻抗 → 變胖。
這套說法因果是倒的。
教科書層的正向因果:
- 阻抗的真正原因是肌肉與肝細胞內異位脂肪堆積 + DAG/ceramide 切斷胰島素訊號
- 因為訊號斷了,葡萄糖才進不去肌肉(餐後肌肉是主要葡萄糖去處),血糖才在血液裡堆高、震盪
換句話說:
| 社群因果模型 | 實際因果方向 |
|---|---|
| 血糖震盪 → 胰島素噴發 → 阻抗 | 異位脂肪 → 訊號斷 → 血糖進不去肌肉 → 血糖在血液裡震盪 |
| 把震盪壓平就能改善阻抗 | 把異位脂肪清掉才能改善阻抗(震盪自然會跟著平) |
CGM 在臨床上有用(追蹤胰島素治療、評估反應、研究用),但不是健康民眾的代謝改善工具。把 CGM 的鋸齒波當治療目標,相當於對著體溫計拼命降溫,沒處理感染源。
實用建議:不必為了 CGM 上那條曲線焦慮。要動的是體重、腰圍、超加工食品、運動、睡眠 — 把異位脂肪清出去,曲線自己會平。
16. 肥胖/瘦不下來就是因為胰島素阻抗?— 因果倒過來
「我瘦不下來,是因為胰島素阻抗 — 胰島素一直叫脂肪儲存、不分解」。聽起來很科學,但因果是倒的。
時序事實:
- 熱量盈餘(任何來源)→ 脂肪累積 → 皮下倉庫接近個人閾值
- 多餘脂肪溢出 → 異位脂肪(肝、胰、肌肉內)
- 異位脂肪 → DAG / ceramide → IRS-1 訊號斷 → 阻抗成立
- 之後阻抗確實會讓代謝狀態惡化、減重變得更困難
胰島素阻抗是肥胖的下游後果,不是原因。把阻抗當「為什麼瘦不下來」的解釋,是話術。
實情:
- 多數人「瘦不下來」的真正原因是熱量平衡(攝取 vs 消耗 + 環境誘因 + 超加工食品 + 睡眠 + 肌肉量 + 壓力 + 遺傳)
- 阻抗嚴重的人代謝率略低、能量分配不利減重;但效應大小被社群誇大
- 治療不是去找「IR 解方」,是處理整體生活型態
結語
健康人:每年健檢看腰圍、空腹血糖、HbA1c、空腹三酸甘油脂、HDL。建立自己的趨勢線比任何單次切點重要。BMI ≥23 + 腰圍超標就該主動加做 OGTT。不必特別花錢驗胰島素阻抗值 — 那不是篩檢工具。
已有前期糖尿病:你正站在最有價值的時間窗。減 5–10% 體重 + 阻力訓練 + 改善睡眠,影響比後來進入糖尿病再處理大得多。重點是減異位脂肪,不是糾結 HOMA-IR 數字。
文獻
教科書
- Williams Textbook of Endocrinology, 15th ed. (2024) — Ch33(T2D 病理生理)
- Williams Textbook of Endocrinology, 15th ed. (2024) — Ch34(T2D 治療)
- Harrison’s Principles of Internal Medicine, 22nd ed. (2025) — Ch415(DM 診斷分類)、Ch411(代謝症候群)
- Harper’s Illustrated Biochemistry, 33rd ed. — Ch42(荷爾蒙訊號傳導)
指引
- ADA Standards of Care in Diabetes — 2026 §2(診斷與分類) · §3 預防、§5 行為與飲食、§9 藥物原始指引見 Diabetes Care Vol 49 Suppl 1 (OA)
- DAROC 2022 第 2 型糖尿病臨床照護指引(中華民國糖尿病學會主指引;附 2024 章節更新:糖尿病足、骨質疏鬆、住院照護)
免責聲明:本文為一般衛教與科普評論,不能取代個別診療。若已有糖尿病、慢性腎臟病、懷孕、使用胰島素或降血糖藥物、有飲食疾患病史,飲食、運動與藥物調整應與醫師或營養師討論。